国立研究開発法人 産業技術総合研究所(以下「産総研」という)触媒化学融合研究センター 官能基変換チーム 生長 幸之助 研究チーム長、吉田 勝 研究センター長は、国立大学法人 東京大学(以下「東大」という)大学院薬学系研究科 金井 求 教授のグループと共同で、低コストで廃棄物を抑えた、ペプチドの大量合成法を実現しました。九つのアミノ酸からなる複雑なペプチドも作製可能です。
人工的にペプチドを大量に作るためには、「化学合成法」が必要です。従来の方法はアミノ酸を特定の順番で一つずつつなげていきますが、保護基を備える高価なアミノ酸原料や活性化剤(縮合剤)を使用するため製造コストが高くなり、廃棄物が大量に生じるために環境への影響も問題となっています。また近年では、保護基を持たないペプチド鎖を反応させる化学選択的ライゲーション法と呼ばれる方法なども、大きなペプチドを効率的に作り出す方法として活用が広まっていますが、その多くは適用できるアミノ酸配列に制限があります。今回、新たに開発したペプチド合成法は、どのようなアミノ酸配列にも適用でき、かつペプチドをブロック単位でつないでいくことで、保護基の使用を抑えながら、大きなペプチドを大量に作ることができます。この実証として、九つのアミノ酸からなる生物活性ペプチドの大量合成に取り組み、成功しました。
この成果は新たな医薬品(中分子医薬品)の開発・供給のみならず、食品・農薬・化粧品・材料などといったペプチドの新たな用途開拓にも貢献します。また、製造コストや環境負荷を抑える合成法は、持続可能な社会の実現に対する一助となります。
なお、この技術の詳細は、2023年10月26日に「Communications Chemistry」に掲載されました。
ペプチドは、いくつかのアミノ酸が鎖状につながった化学物質です。特に5~10個のアミノ酸がつながった人工ペプチドは、新しい医薬品(中分子医薬品)への応用が期待されています。これらのペプチドを人工的かつ大量に作るためには、「化学合成法」を使うことが一般的です。
現在のペプチド化学合成法は、アミノ酸の一部から始めて、カルボン酸末端からアミン末端に向かう(C-to-N)方向に、他のアミノ酸を一つずつ順番につなげてペプチド鎖を伸ばしていく方法が一般的です。しかし、この方法では、アミノ酸を正確につなげるために、多数の「保護基」を使う必要があります。保護基を備えたアミノ酸は高価であり、原料として用いることは製造コストを上げる原因となっています。さらに、アミノ酸をつなげるためには、「縮合剤」と呼ばれる活性化剤も原料と同量以上に必要です。保護基と縮合剤は、反応が終わった後に廃棄物となるため、環境負荷を増大させます。
このような理由から、大量のペプチドを作ると、環境への負荷や製造コストが高くなってしまう問題があります。また、現在の方法では、アミノ酸を一つずつ順番につなげていくしかありません。複雑なペプチドをつなげてさらに大きなペプチドを作ることができれば、合成効率を大幅に上げられる可能性があります。しかし、この方法では複雑なペプチドに含まれる構造や部品の向きが反応の途中で変化し、目的としない生成物を与える「エピメリ化」という副反応が起こりやすいため、その実現は困難です。
ペプチド化学合成法におけるコスト・廃棄物・合成効率についての問題を解決するために、アミン末端からカルボン酸末端(N-to-C)へ、つまり従来法(C-to-N)とは逆方向にペプチド鎖を伸ばしていく方法を多くの化学者が実現しています。しかし、このN-to-C合成法には副反応を抑制することが難しいという問題がありました。これを解決するために、東大の金井 求 教授らはペプチドカルボン酸をペプチドチオカルボン酸(peptide thiocarboxylic acid, PTC)に変換し、保護基を持たないアミノ酸をつなげることを繰り返すことで、逆方向にペプチド鎖を伸ばしていく合成法を開発しました(図1、図2)。PTCを利用する方法では、保護基や縮合剤に由来する廃棄物が少なく抑えられます。従来用いられてきた順方向の合成法では、n個のアミノ酸を伸ばす過程でn個分の保護基が必要になります。一方、逆方向の合成法ではアミノ酸1個分だけあればよいため、廃棄物を減らすことができます。また、PTC化剤も、従来の縮合剤に比べてサイズが小さいので、これも廃棄物を減らすことに貢献します。保護基を持たないアミノ酸やPTC化に用いられる反応剤は、いずれも安価に購入できるため、製造コストも低く抑えられます。さらには、独自開発された添加剤(HOPOPhy)を使用することで副反応を抑えることができ、添加剤は使用後に回収・再利用が可能です。
この逆方向合成法の確立により、安価な無保護アミノ酸を使って、副反応をほとんど起こさず、ペプチド鎖を一つずつ伸ばしていく大量合成が可能になりました。(図2,特開2021-130656)。
なお、本研究開発の一部は、独立行政法人日本学術振興会の科学研究費助成事業「基盤研究S(2023~2027年度)」および「学術変革領域研究B(2021~2023年度)」による支援を受けています。
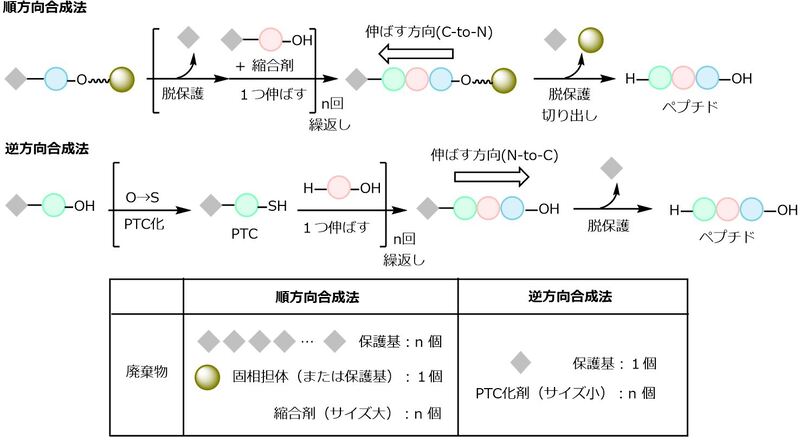
図1 順方向合成法と逆方向合成法の比較
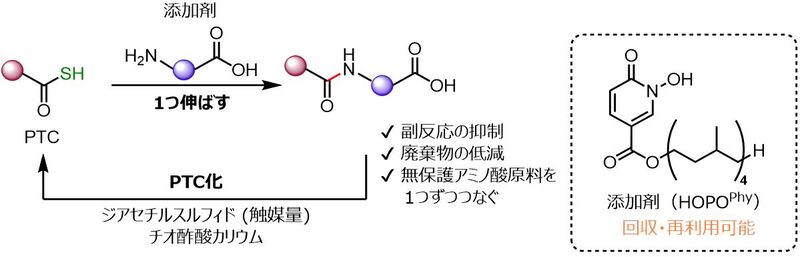
図2 ペプチドチオカルボン酸(PTC)を経由するペプチド合成法
今回、産総研の生長 幸之助 研究チーム長らの研究グループと東大の金井 求 教授らは、これまでの研究を発展させて、大きなペプチドを人工的に合成するための新たな方法を開発しました。あらかじめ複雑なペプチドの部分構造となる分子を作製し、これらをブロック単位としてつなげていくことで、より大きなペプチドを作る手法です。すなわち、複数のアミノ酸がつながったペプチドブロックをPTCに変換し、それに対して保護基を持たない別のペプチドブロックをつなげるという手順を用いることで、大きなペプチドを作りました。つまり、一つずつアミノ酸を伸ばすのみならず、ブロック単位でも同じ考え方(N-to-C)でつないでいけることを実証しました(図3)。これまでの技術では、複雑なペプチド同士をつなげようとすると、適用可能なアミノ酸配列に制限があったり、副反応(エピメリ化)が起こりやすかったりという問題がありました。今回、PTC経由でつなぐ考え方をブロック単位でも示したことで、この問題を解決しました。この研究によって、大きなペプチドを効率的に作るための基盤技術を確立することができました。
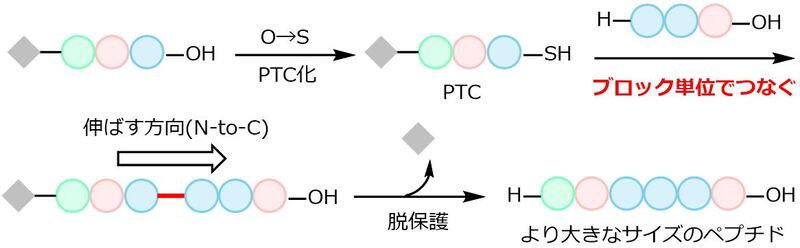
図3 逆方向合成法を発展させた、ブロック単位でつなぐ新しいペプチド合成法
この新しい合成法の有用性を実証するために、複雑な生物活性ペプチドであるDelta Sleep-Inducing Peptide(DSIP)を合成しました。DSIPは、九つのアミノ酸がつながった神経ペプチドで、抗不安作用を示します。
今回の研究ではまず、アミノ酸を一つずつ伸ばしていく合成法(N-to-C)を用い、それぞれ三つのアミノ酸がつながった3種のペプチド断片(断片1・断片2・断片3)を用意しました。それぞれのペプチド断片は、保護基の使用を最小限にしながら、グラムスケールで作ることが可能でした。その後、図3に示したように、ブロック単位のペプチド断片を順番につなげていきます。最後に、全ての保護基を一度に取り除くことで、全19工程にて、目的物質であるDSIPの合成と、100 mg以上・90%精製純度以上での単離に成功しました。合成過程で使用した添加剤(HOPOPhy)は、使用後に回収・再利用が可能でした。実際の合成反応を図4に示します(W, A, G, D, S, Eは、それぞれペプチドを構成するアミノ酸1単位を意味しています)。今回開発された新しい合成法により、最小限の保護基の使用で、複雑なペプチドを効率的に作れることが示されました。これはペプチドの製造化学における大きな進歩であり、新しい医薬品の開発と供給に大きく貢献します。また、ブロック単位で反応させると合成効率が上がるため、この新たな手法は、ペプチドの製造において環境負荷や製造コストを減らすとともに、副反応を抑えることで品質管理面での課題を解決し、持続可能な社会の実現にも寄与することが期待されます。
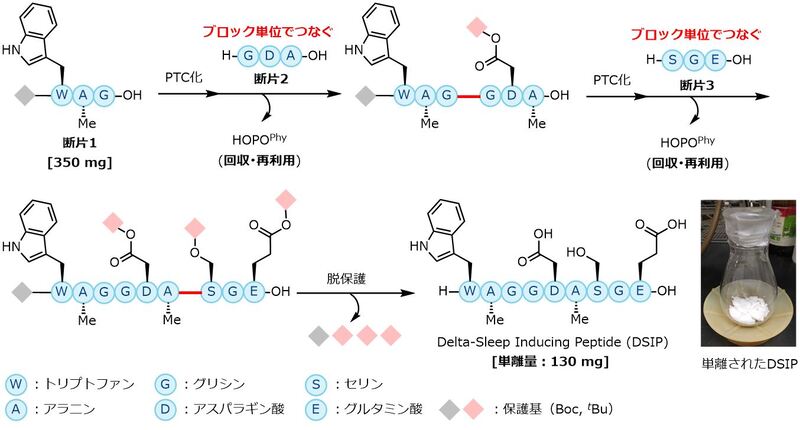
図4 複雑な生物活性ペプチドの大量合成
※本プレスリリースの図2と図4は原論文の図を引用・改変したものを使用しています。
この新しい合成法は、食品・農薬・化粧品・材料など、これまでペプチドが活躍できると思われていなかった産業でも、ペプチドを応用・実用していく道を拓くことが期待されます。このために、新しいペプチド製造技術を持つスタートアップ企業の設立や、大学や化学製品企業とのさまざまな分野での共同研究を進め、ペプチドが活躍できる新たな市場開拓を目指す予定です。
掲載誌:Communications Chemistry
論文タイトル:Practical N-to-C peptide synthesis with minimal protecting groups
著者:Toshifumi Tatsumi, Koki Sasamoto, Takuya Matsumoto, Ryo Hirano, Kazuki Oikawa, Masato Nakano, Masaru Yoshida, Kounosuke Oisaki*, Motomu Kanai*
DOI:10.1038/s42004-023-01030-0