独立行政法人 産業技術総合研究所【理事長 野間口 有】(以下「産総研」という)バイオメディシナル情報研究センター【研究センター長 嶋田 一夫】機能性RNA工学チーム 廣瀬 哲郎 研究チーム長、細胞システム制御解析チーム 夏目 徹 研究チーム長らは、ヒト細胞核中のU7核内低分子RNA(U7 RNA)が、細胞内の状態に応じて、二つの相反する遺伝子発現制御を行うことを発見した。
U7 RNAは、DNAと共に染色体を構成するヒストンというタンパク質の遺伝子発現制御にかかわっている。ヒストンは、細胞核内で新しい染色体が形成されるDNA複製期(S期)にだけ合成される。これまでU7 RNAは、S期にヒストンの遺伝子発現を促進する「正」の制御を行うことが知られていた。今回、S期以外のDNA複製が起こっていない細胞のU7 RNAの機能を解析し、ヒストン遺伝子の発現が起こらないように「負」の制御を行っていることを見いだした。
これによって、特定の時期に細胞内で必要となるタンパク質を、その時期にだけ合成するために、同一のRNAが遺伝子発現の促進と抑制の両面を使い分ける巧妙なシステムが存在することが分かった。さらにこの発見は、RNAの機能を利用した遺伝子機能の制御技術など、創薬開発に貢献することも期待される。
詳細は、The Proceedings of the National Academy of Sciences of the United States of America(PNAS、米国科学アカデミー紀要)電子版に掲載される。
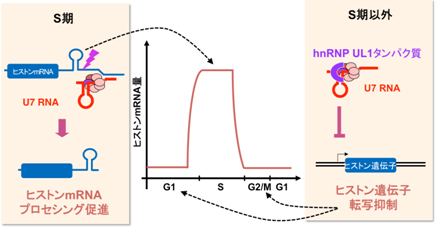 |
| 図1細胞状態に応じたU7 RNAによるヒストンの遺伝子発現制御 |
ヒトゲノム解析によって、ヒトのタンパク質遺伝子の数が、マウスのものとほとんど変わらないことが分かった。一方でポストゲノム研究によって、ヒトゲノムやマウスゲノムの大部分から、機能の分からないRNAが多数生産されていることが明らかになった。これらのRNAはタンパク質に翻訳される情報を含まない「ノンコーディングRNA」と呼ばれ、主に細胞核内で機能すると考えられている。最近一部のノンコーディングRNAが、遺伝子発現の制御や細胞内構造形成、さらには疾患の発症にかかわることが明らかにされ、RNAの制御機能に注目が集まっている。
産総研では、ノンコーディングRNAの中から重要な機能を果たす「機能性RNA」の発見と、その応用技術開発を目指している。これまでに細胞核内におけるRNA機能の解析のための手法を開発し、RNAの新機能探索を進めてきた。
なお、本研究開発は、独立行政法人 日本学術振興会の先端研究助成基金助成金「最先端・次世代研究開発支援プログラム(平成22~25年度)」による支援を受けて行った。
DNAに結合して染色体を構成するヒストンというタンパク質は塩基性が強く、結合するDNAがなくて単独となった過剰なヒストンは、細胞にとって有害である。そのためヒストンの遺伝子は、細胞内のDNA複製時期(S期)にだけ発現するように厳密に制御され、細胞核内で新しい染色体が形成されるS期にのみヒストンが合成される(図1中央)。細胞核内に局在するU7 RNAは、ヒストン遺伝子のmRNAプロセシングを促進することによって、S期のヒストン合成に寄与している(図1左)。一方、U7 RNAは、S期以外のDNA複製が起こっていない時期にも豊富に存在していることが知られていた。
今回、S期以外の細胞を用いて、U7 RNAだけを、アンチセンス核酸によって分解したところ、通常なら発現が抑制されているヒストン遺伝子の転写が著しく上昇した。またU7 RNAを過剰に細胞内で合成させると、逆にヒストン遺伝子の転写を抑制できた。これらの結果からS期以外の細胞では、U7 RNAはヒストン遺伝子発現を抑制し、余分なヒストンを作らないように制御していることが分かった(図1右、表1)。
| 表1 U7 RNAの二つの機能によるヒストン遺伝子発現制御 |
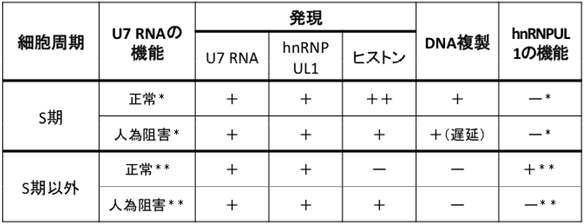 |
| 「*」はヒストンmRNAプロセシング促進機能、「**」はヒストン遺伝子転写抑制機能が働いていることを示す。「+」は発現・DNA複製・hnRNPUL1タンパク質の機能があることを示し、
「++」は、特に強いことを示す。「-」はそれらがないことを示す。
|
ヒストン遺伝子発現を抑制するため、U7 RNAは特異的なタンパク質と複合体を形成していると考えられた。そこで、U7 RNAに結合しているタンパク質を高感度質量分析によって探索した結果、hnRNPUL1タンパク質を新たに同定した。hnRNPUL1タンパク質の機能阻害実験、過剰発現実験を行ったところ、U7 RNAの機能解析と同様に、ヒストン遺伝子の転写を制御することが確認できた。また、hnRNPUL1タンパク質が抑制機能を発揮するには、U7 RNAが必要であった(図1右、表1)。一方、hnRNPUL1タンパク質を機能阻害したところ、U7 RNAによるS期のヒストン合成は影響を受けず、U7 RNAの転写抑制機能のみに異常が現れたことから、このhnRNPUL1タンパク質は、U7 RNAの転写抑制機能だけに関与するタンパク質因子であることが分かった(表1)。
このように、U7 RNAは、S期にはヒストン合成を促進し、S期以外にはヒストン合成を抑制するという二つの重要な役割を担っている。こうしたRNA機能を利用することにより、発現強度を段階的に調節できる人工遺伝子スイッチの開発などの応用が期待される。
U7 RNAの二つの機能のメカニズムの詳細を解明する。さらに、どのようにして細胞状態を感知して機能を転換できるのかを明らかにする予定である。また、ヒストン遺伝子以外のU7 RNAの標的を探索/同定することを目指す。