- 生体内において設計したパターン通りに短時間で細胞を配置できるマイクロマシンを開発
- 治療用の幹細胞を潰瘍性大腸炎モデルマウスの腸内に配置できることを実証
- 従来の幹細胞治療を発展させ、より正確で確実な組織の再生を可能に
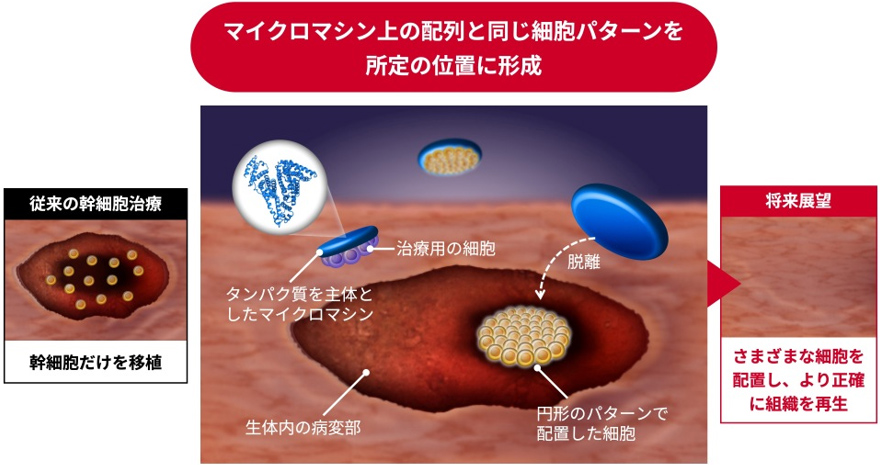
マイクロマシンを用いた生体内での細胞配置
※原論文の図を引用・改変したものを使用しています。
国立研究開発法人 産業技術総合研究所(以下「産総研」という)モレキュラーバイオシステム研究部門 山添泰宗 主任研究員、細胞分子工学研究部門 寺村裕治 研究グループ長と、兵庫医科大学 医学部 消化器内科学 新﨑信一郎 主任教授は、タンパク質を主体としたマイクロマシンを用いて生体内の所定の位置に望みのパターンで細胞を配置する技術を開発しました。
幹細胞治療とは幹細胞を病変部に移植し、幹細胞の持つ分化能と自己複製能を利用して、損傷した組織の修復や失われた機能の再生を目指すもので、世界中で技術開発や臨床試験が進んでいます。しかし、病変部に幹細胞を移植するだけの現状の方法では、多種の細胞が関与する複雑な組織修復の工程を厳密に制御できず、確実かつ正確に正常組織を再生することは困難でした。もし病変部にさまざまな細胞を望み通りに配置することができれば、多種類の細胞が連携しながら進行する組織修復の工程や、生体の複雑な組織構造を考慮した正確な組織再生が可能になると期待されますが、生体内に細胞を望み通りのパターンで配置する技術は開発されていませんでした。
生体内に細胞を配置する場合、安全性の確保に加え、体への負担を減らすため、低侵襲な手法により極力短い時間で配置操作を行うことが重要です。今回、これらの条件を満たしながら、生体内の所定の位置に望みのパターンで細胞を配置できるマイクロマシンの開発に成功しました。そして、このマイクロマシンを用いて、実際の応用を想定し、潰瘍性大腸炎モデルマウスの損傷した腸組織に治療効果のある間葉系幹細胞を設計したパターンで配置できることを実証しました。開発したマイクロマシンの表面には、細胞膜に挿入される性質を持つ細胞捕捉ユニットが結合しており、これにより細胞を捕捉して目的地に輸送後、30分という短時間でその場に脱離することで、所定の位置にマイクロマシンと同じ形の細胞パターンを形成させます。
本方法では、パターンを形作る多数の細胞を一括して配置するため、細胞を1個ずつ並べて目的のパターンを作製する場合と比べて、より早く簡便に望みの細胞パターンを作製することができます。また、微小なマイクロマシンを用いているため、低侵襲で細胞を配置することが可能です。
この生体内細胞配置技術は、幹細胞移植後の組織修復工程を意図的に制御して精密に組織を再生する道を切り拓き、幹細胞を用いた再生医療の前進に貢献すると期待されます。
今回の研究成果の詳細は2025年12月17日に「Materials Today Bio」にオンライン掲載されました。
現在、医療分野では、さまざまな細胞に変化できる幹細胞を利用した再生医療が大きな注目を集めています。これは、病気やけがで失われた組織を修復し、より根本的な治癒を目指すものです。腸、血管、脳、心臓、肝臓などさまざまな臓器で研究が進んでいますが、既存の治療法は、病変部への幹細胞の単なる移植にとどまり、細胞の働きや組織再生プロセスを厳密に制御できていません。いわば、幹細胞に任せきりになってしまうという問題がありました。
一方、生体組織工学(Tissue Engineering)の分野では、生体組織の細胞配列のパターンを模倣しながらさまざまな細胞を基板上に配置し、薬の評価や移植治療に利用できる人工的な組織を作る研究が活発に行われています。
われわれは、この生体組織工学の分野の細胞配置技術に着目しました。この技術を応用し、病変部にさまざまな細胞をあらかじめ設計したパターンで配置することで、組織再生プロセスを意図的に制御し、より正確に組織を再生させることを考えました。しかし、従来の細胞配置技術は、インクジェットプリンターを用いて細胞を吐出して配置する方法や、光照射を利用して照射部に細胞を配置する方法など、体外(基板上)での使用を想定して開発されているため、そのまま生体へ適用することはできません。さらに生体内での細胞配置では、安全性の確保に加え、体への負担を減らすため、低侵襲な手法により極力短い時間で配置操作を行うことが求められます。これらの制約を満たす新たな細胞配置法を開発する必要がありました。
産総研では、磁力で遠隔操作できるマイクロマシンを用いた細胞の輸送・配置技術を開発しています。これまで、基板上に細胞を配置し、複数の細胞から成る細胞構造体を作製できることを示し、報告してきました(2020年2月12日 産総研主な研究成果)。今回、このマイクロマシンを発展させ、生体内において細胞を配置する方法の確立に取り組みました。
産総研で開発を進めているマイクロマシンは、生体に異物として認識され有害な生体反応を引き起こす金属や合成高分子などを用いず、医薬品にも使用されているタンパク質(血清アルブミン)を主な材料として作製しています(2017年11月17日 産総研プレス発表)。また、磁気応答性を付与するために含有させている磁性体も、MRIの造影剤で使用されている安全性の高い酸化鉄ナノ粒子(マグヘマイト)を用いるなど、効果的かつ低侵襲で安全な次世代医療の理想形を目指して研究を進めています。
なお、本研究開発は、独立行政法人 日本学術振興会の科学研究費助成事業(23K25219、25K03474)による支援を受けています。
図1aに開発したマイクロマシンを示します。安全で均質なマイクロマシンを作製するため、リコンビナント技術により大量生産された医薬品グレードのヒト血清アルブミンを用いて本体部を作製しました。また、外部から印加した磁場によって遠隔で動かすことができるように、磁性ナノ粒子を含有させています。今回、体外に設置した磁石で、離れた距離にあるマウス腸内のマイクロマシンを操縦するため、より多くの磁性ナノ粒子を含有させました。マイクロマシンの表面には、細胞の「捕捉」と「脱離」を担う細胞捕捉ユニットを結合させています。ユニット先端部のオレイル基が疎水相互作用によって細胞膜に挿入され、細胞を捕捉します(図1b)。一方、タンパク質溶液を加えると、細胞膜からオレイル基が脱離して添加されたタンパク質に結合するため、マイクロマシンは捕捉していた細胞を脱離します。
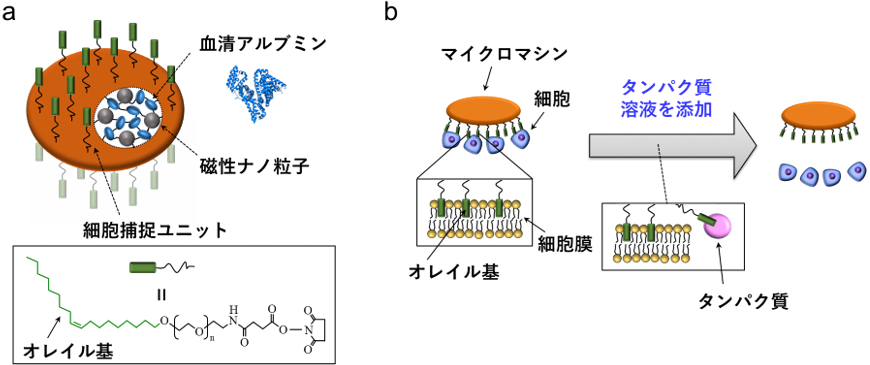
図1 (a)開発したマイクロマシン(b)マイクロマシンによる細胞の捕捉と脱離
※原論文の図を引用・改変したものを使用しています。
マイクロマシンを用いた標的部への細胞配置は次の手順で行います(図2)。①細胞を捕捉したマシンを磁力を利用して標的部に運ぶ、②運んだ細胞をその場に強く密着させて物理吸着させる、③タンパク質溶液に暴露しマシンから細胞を脱離させる。この配置操作により、標的部にマイクロマシンと同じ形状の細胞パターンが形成されます。
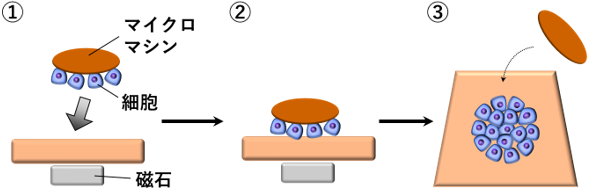
図2 マイクロマシンを用いた細胞配置の手順
※原論文の図を引用・改変したものを使用しています。
生体内に細胞を配置する場合、生体への負荷を減らすために、極力短時間で配置操作を終える必要があります。配置に要する時間はマイクロマシン表面の細胞捕捉ユニットの数に左右されます。ユニットが多いと、確実に細胞を捕捉できるものの、脱離に時間がかかります。逆に、少ない場合は、素早く脱離できますが、細胞を十分に捕捉できません。そこで、さまざまな密度でユニットを結合させたマイクロマシンを作製し、マシンの細胞捕捉能と、タンパク質溶液に一定時間暴露した際のマシンからの細胞の脱離挙動を検証しました。その結果、確実な捕捉と短時間(30分)での脱離を実現するために、間葉系幹細胞と線維芽細胞ではマシンに結合させるユニット密度が1.8倍違うことが分かりました(図3a)。また、マシンに捕捉された細胞の面積は、間葉系幹細胞では、線維芽細胞に比べて2.2倍大きいことが分かりました。これらの結果は、どちらの細胞でもほとんど同じ数のユニット(約2×107個/1細胞)で捕捉されうることを示しており、今後多様な細胞に対応したマイクロマシンを開発するうえで重要な指針になります。図3bに線維芽細胞を捕捉した円形のマイクロマシンの様子を示します。マシン全面に良好に細胞が捕捉されていることが分かります。
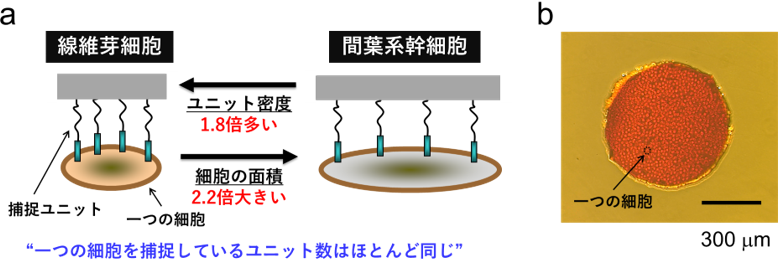
図3 (a)個々の細胞に適した細胞捕捉ユニットの検証(b)線維芽細胞を捕捉したマイクロマシン
※原論文の図を引用・改変したものを使用しています。
作製したマイクロマシンを用いて、30分という短時間で標的部に細胞を望みのパターンで配置することができました。図4aに円形のマイクロマシンを用いて、間葉系幹細胞を生体組織のモデルとなるゲル(マトリゲル)上に円形パターンで配置した結果を、また図4bにリング型のマイクロマシンを用いて、線維芽細胞を異種の細胞(ストローマ細胞)上にリング状パターンで配置した結果を示します。
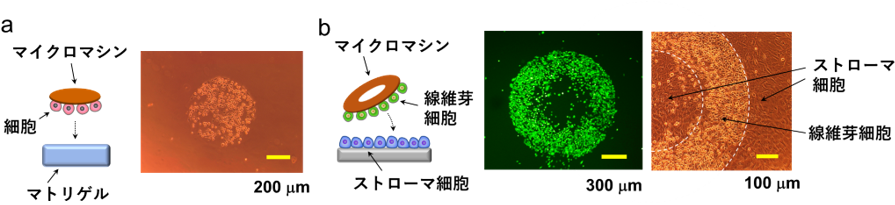
図4 (a)マトリゲル上への細胞配置(b)異種の細胞上への細胞配置、形成された細胞パターンの蛍光顕微鏡像(左)とその拡大像(位相差顕微鏡像、右)
※原論文の図を引用・改変したものを使用しています。
次に、マイクロマシンを用いて潰瘍性大腸炎モデルマウスの損傷した腸組織に治療効果がある間葉系幹細胞の配置を行いました(産総研の動物実験に関する倫理委員会のガイドラインに従って実施)。図5aにマイクロマシンを用いた腸内での細胞配置の概要を示します。微小なマイクロマシンを長距離にわたって磁力による遠隔操作で操縦し、体内の目的地に到達させるのは現在の技術では困難です。そこで今回、内視鏡を用いて腸内の標的部の真上であらかじめ間葉系幹細胞を捕捉させておいたマイクロマシンを放出し、体外に設置した磁石で引き寄せることで、磁力によるマイクロマシンの操作区間をごく短い距離に限定して標的部にマイクロマシンを到達させました。図5bは、腸内に導入した直径約0.5 mmの円形のマイクロマシンです。マイクロマシンから細胞を脱離させ、腸組織に細胞を配置した様子を図5cに示します。間葉系幹細胞の円形パターンが観察され、マウスの腸内においても短時間で望みのパターンで細胞を配置することができました。なお、細胞配置後のマイクロマシンは、排泄物と一緒に体外に排出されます。
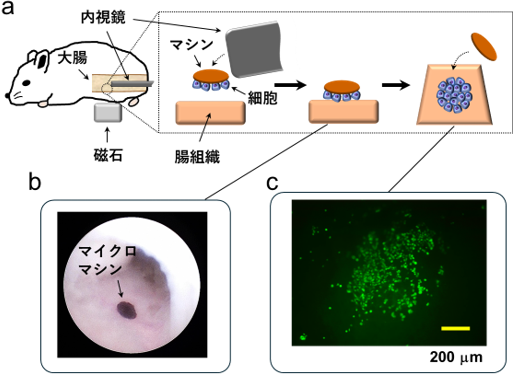
図5 (a)マイクロマシンを用いたマウス腸内での細胞配置の手順(b)腸内に導入したマイクロマシンの内視鏡像 (c)腸組織に円形パターンで配置された間葉系幹細胞
※原論文の図を引用・改変したものを使用しています。
今回、タンパク質を主体とした安全性の高いマイクロマシンを用いる低侵襲な手法により、生体内の所定の位置に短時間で細胞を配置することに成功しました。この生体内細胞配置技術を利用することで、「どのような細胞を、どのように配置すれば正常組織が再生するか」という知見を得ることができます。この知見をもとに、幹細胞による組織修復を意図的に制御することで、より正確で確実な正常組織の再生を実現できると期待されます。
今後は、生体内に配置した細胞による組織修復作用に関する研究に取り組み、効果的に組織を再生する高度な幹細胞治療に向けた研究を進めます。
掲載誌:Materials Today Bio
論文タイトル:Cell patterning in vivo using microrobot specifically designed for tissue engineering applications
著者:Hironori Yamazoe, Yoshiaki Yamano, Yuji Teramura, Shinichiro Shinzaki
DOI:10.1016/j.mtbio.2025.102683