- PEG脂質による血管内皮のコーティング技術をブタ腎臓に適用し、ブタの腎移植実験において免疫反応を抑制
- 臨床でのヒト腎移植にも適用できる最適なコーティング条件を明確化
- ヒト腎移植の長期生着率の向上を目指し、臨床試験が進行中
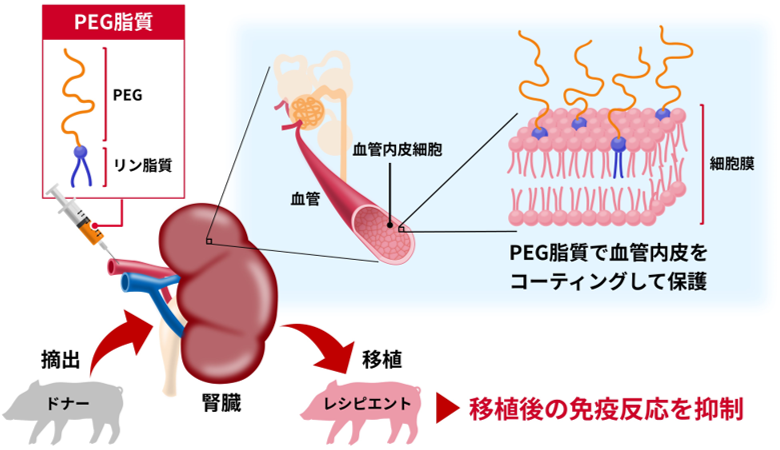
概要図 両親媒性ポリマー(PEG脂質)で血管内皮コーティングしたブタ腎臓の移植実験
国立研究開発法人 産業技術総合研究所(以下「産総研」という)細胞分子工学研究部門 細胞制御マテリアル研究グループ 寺村裕治 研究グループ長とスウェーデンのiCoat Medical社、ウプサラ大学らは共同で、腎臓の血管内皮を両親媒性ポリマーでコーティングすることによって、腎移植後に起こる虚血再灌流障害を抑制する技術を開発しました。
腎移植は重症の腎疾患患者が人工透析を回避できる唯一の治療法で、移植した腎臓が長期にわたって患者の体内で生着することが重要です。そのためには移植時に起こる、臓器の損傷を引き起こす免疫反応を抑制する必要があります。本研究では、ポリエチレングリコール(PEG)とリン脂質との結合体である両親媒性高分子、PEG脂質によるコーティング技術を腎臓内の血管内皮表面に適用することで、腎移植後に起きる免疫反応の一つである虚血再灌流障害が抑制されることを、ブタを用いた動物実験により明らかにしました。
この成果の詳細は、2025年9月24日にAmerican Journal of Transplantation誌に掲載されます。
さらに、今回のブタの腎移植実験をはじめとする技術開発の過程において、臨床でのヒト腎移植にも適用できるコーティングの最適条件を明確化しました。ヒト腎移植の生着率を大きく下げる虚血再灌流障害を効果的に抑制できる薬剤は現在までに見いだされておらず、移植外科の経験と手技に大きく依存しています。開発したコーティング技術はヒト腎移植の生着率向上に寄与すると期待され、現在、本技術を活用した臨床試験を進めています。
日本における慢性腎臓病の患者数は2000万人と推計され、このうち人工透析を必要とする患者数は2022年末時点で35万人とされています※1。透析患者は1回4時間の血液透析を週3回受けなければならず、QOL(Quality of life:生活の質)は著しく低下します。また、人工透析を行っている患者は、合併症を患いやすく、心不全や糖尿病で亡くなるケースが多い上に、高額な医療費が患者本人にとっても国庫にとっても負担になっています。
腎疾患患者は、腎機能低下を阻止できない場合に人工透析や腎移植による治療を行う必要が出てきますが、治療開始後の10年生存率は腎移植のほうが優れるという報告があります※2、3。2020年10月のWHOの報告書では、世界でおよそ9.5万件の腎移植が行われており、その数は年々増加しています※4。腎移植は最も事例の多い移植医療として定着しつつあります。一方、移植した腎臓が、長期間にわたって患者の体内で生着して機能しなければ、数年後には再移植を余儀なくされますが、現状ではドナーの数は十分とは言えず、再移植を受けることが難しい状況になっています。そのため、移植した腎臓を、患者の体内で安定に生着させる薬剤や技術が求められています。
これまでの研究から腎臓を移植した直後に起きる虚血再灌流障害が、生着率を下げる要因の一つであることがわかっています。虚血再灌流障害は腎移植直後に起こる免疫反応の一つで、自然免疫の活性化と血液凝固反応の活性化、活性酸素の発生などが複雑に関与して、移植した腎臓の細胞や組織に障害をもたらします。そのため、一つの薬剤で制御することは困難であり、虚血再灌流障害を効果的に抑制できる薬剤や技術は見いだされていません。
産総研はこれまでに、組織並びに臓器や組織内の血管表層の改変を行うために、さまざまな種類のPEG脂質を利用した細胞のポリマー修飾や薄膜カプセルの検討を行ってきました。今回、PEG脂質によるコーティング技術が、ヒト腎移植に適用可能かを検討するために、ヒトと相同性の高いブタの腎臓を対象として、血管内皮や組織のコーティングに適したPEG脂質のPEG分子量と脂質の組成を慎重に検討し、ブタ腎移植モデルを用いた検証を行いました。
本研究開発は、スウェーデンのウプサラ大学とiCoat Medical社との共同研究として実施しました。
今回、細胞表面を保護するポリマーとして、PEGとリン脂質との複合体である“PEG脂質”を開発しました。リン脂質部が細胞膜の脂質二重層と疎水性相互作用を生じることで、細胞表面へ導入されるため、PEG脂質による細胞のポリマーコーティングが可能になります(概要図)。この技術を利用して、ブタ腎臓内の血管内皮表面のPEG脂質コーティングを試みました。ドナーブタから摘出した腎臓の動脈にPEG脂質溶液を注入することで、腎臓内の血管内皮表面へPEG脂質が導入され(概要図)、この腎臓をレシピエントブタへ移植しました(図1)。分子量5 kDaのPEG分子と、脂質としてジパルミトイルホスファチジルエタノールアミン(DPPE)を複合化させたPEG脂質を導入したところ、腎臓の血管内皮を効果的にコーティングできることを確認しました。このPEG脂質による血管内皮のコーティングでは、およそ5 nm程度の高分子薄膜が形成され、細胞膜や表面レセプターを被覆できます(図2)。また、腎臓の血管内皮のコーティングは、低温(氷上)かつ1時間以内の処理で可能であることが分かりました。臨床現場では、移植する臓器中の細胞生存時間を考慮すると、低温かつ短時間の処理が求められますが、今回のコーティング条件であれば、臨床でのヒト腎移植にも適用しうるプロトコールを確立できます。
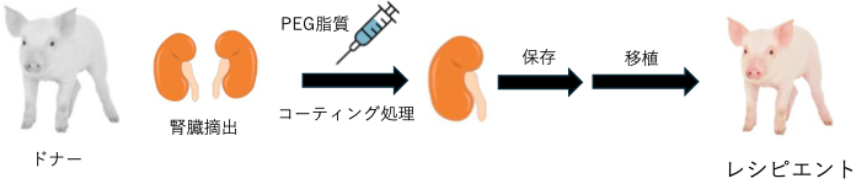
図1 本研究で実施したブタ腎移植の概要。ドナーとなるブタから腎臓を摘出し、残存している血液を完全に取り除き洗浄する。その後、PEG脂質を動脈から注入して、氷上で反応させた後、レシピエントのブタへ移植する。
※原論文の図を引用・改変したものを使用しています。
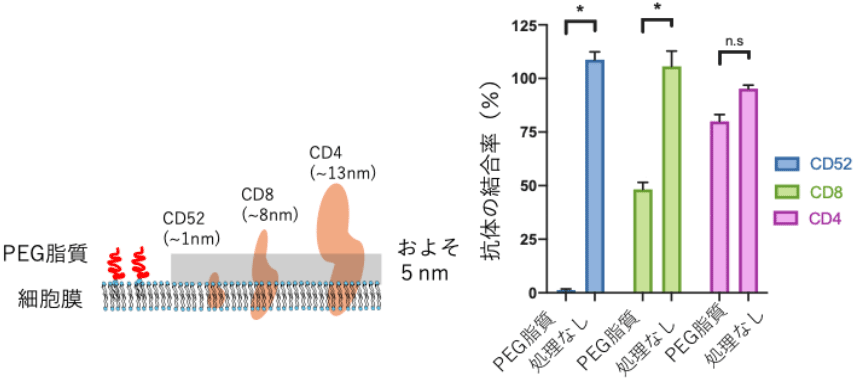
図2 細胞表面にコーティングされたPEG脂質に関する分析結果。細胞をコーティングした後、表面抗原に反応する3種類の抗体(CD4、CD8、CD52に対する抗体)の反応性を調べた。PEG脂質でコーティング処理すると、サイズの小さいCD52に対する抗体はほとんど反応せず、完全に保護できている。しかし、PEG脂質の厚さよりも大きいレセプター(CD8やCD4)に対してはコーティングの効果が薄れる。このことから、細胞表面でのコーティングの厚みは、およそ5 nm程度と推察している。
※原論文の図を引用・改変したものを使用しています。
次に、コーティング処理した腎臓の効果を調べるために、腎移植後6時間と4日間の経過観察を行なったブタ腎移植モデルを用いて、移植後の評価を行いました(図3)。レシピエントブタにコーティング処理した腎臓を移植すると、移植直後にはコーティング膜は腎臓内で残存しており、半減期が14時間で、移植2日後にはほぼ消失することが確認できました。これは細胞膜に導入されたPEG脂質が徐々に脱離していくためと考えられます。移植後4日間経過のレシピエントブタの血液検査を行ったところ、コーティング処理有りのグループでは、補体系(C3a、sC5b-9)と凝固系パラメーター(TAT)、サイトカイン類(TNF、IL-1β、IL-2、IL-4、IL-6、IL-10、IL-12、IL-18、IFN-γ)の値が、コーティング処理無しのグループと比較すると、統計的に有意に低いことが分かりました(図3左)。このことは、移植直後に起きる自然免疫が中心となる免疫反応の活性化や凝固反応が抑制されていることを示しています。また、腎機能の指標となる血漿クレアチニンを測定したところ、コーティング処理有りのグループではクレアチニンの値が統計的に有意に低く、移植後の腎機能が迅速に回復したことが示されました(図3右)。これらの結果から、コーティング処理有りのグループでは免疫系からの攻撃を防御することで、細胞機能の保護や血栓形成が回避でき、移植した腎臓が相応に機能していることが示唆されました。
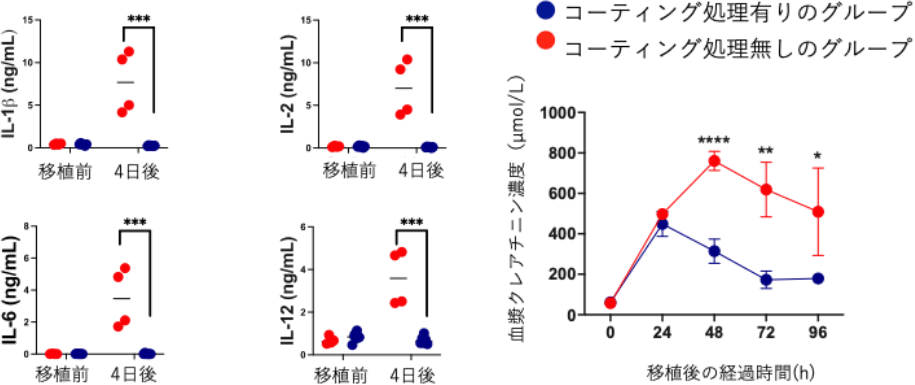
図3 PEG脂質でコーティング処理した腎臓をレシピエントのブタへ移植した後の分析結果。ドナーから摘出した腎臓に対して、PEG脂質でコーティング処理したグループ(青)と処理なしのグループ(赤)を比較した。移植4日後のレシピエントブタの血液中のサイトカイン類(IL-1β、IL-2、IL-6、IL-12)を調べると、コーティング処理有りのグループは処理無しのグループに比べ、サイトカイン類の血中の値が低く、免疫反応が抑制されていることが示唆されている。また、腎機能を反映する血漿クレアチニンにおいても、コーティング処理したグループで低い値を示したことから、移植後の腎臓が機能していることを示している。
われわれのアプローチでは、ポリマー材料であるPEG脂質によるコーティングで、免疫反応による細胞膜への攻撃を物理的に遮蔽し、一時的なバリアーを作成することで、虚血再灌流障害による細胞傷害を抑制できました。
今後、臨床でこのPEG脂質コーティングの安全性が確認され、腎移植への適用が進めば、移植直後に起こる虚血再灌流障害による影響を軽減し腎臓を保護できるため、長期生着率の向上が期待できます。それは患者のQOLの維持に貢献し、再移植や人工透析に戻る可能性を下げることにもつながると考えられます。
今回開発したPEG脂質溶液を臓器保存液として展開することで、ドナーから摘出した臓器の臨床での生着率の向上が可能になると期待されます。すでに、2022年から2023年にかけて、スウェーデン国内で患者18人を対象として、腎移植の臨床試験(Phase I/IIa)を実施し、臓器保存液としての安全性と有効性を調べました(米国ClinicalTrials.govでの登録番号:NCT05246618)。今後、安全性と有効性について大規模な試験により検証するために、欧米での臨床試験(Phase IIb/III)に進める予定です。また、本コーティング技術は腎移植だけでなく、他の移植医療や細胞移植にも適用可能であるため、今後は本技術を応用し、移植医療や再生医療の実現に貢献したいと考えています。
掲載誌:American Journal of Transplantation
論文タイトル:A new principle to attenuate ischemia reperfusion injury in kidney transplantation
著者:Ali-Reza Biglarnia*, Yuji Teramura*, Sana Asif, Claudia Dührkop, Vivek Arnand Manivel, Elin Manell, Patricia Hedenqvist, Anneli Rydén, Felix Sellberg, Karin Fromell, Sabine Hammer, Markus Huber-Lang, Kristina N Ekdahl, Marianne Jensen-Waern, Bo Nilsson (*equally contributed)
DOI:10.1016/j.ajt.2025.08.024
※1 CKD診療ガイド2024 日腎会誌 2025:67(1):1-178
※2 2023年度版 腎不全 治療選択とその実際
※3 我が国の慢性透析療法の現況(2015年12月31日現在)
※4 一般社団法人 日本移植学会 日本移植学会のファクトブック2020 Fact Book 2020 on Organ Transplantation in Japan