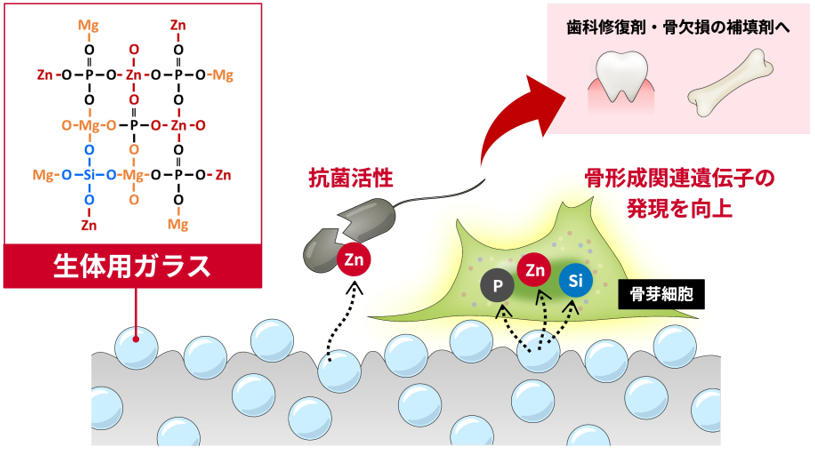
- オルト四面体のみで構成される生体材料向けMgO-ZnO-P2O5-SiO2系ガラスを開発
- 亜鉛イオンの適度な溶出により優れた抗菌活性と骨形成促進機能を両立
- 骨形成関連遺伝子の発現を向上する生体適応材料として期待
※原論文の図を引用・改変したものを使用しています。
国立研究開発法人 産業技術総合研究所(以下「産総研」という)マルチマテリアル研究部門 李 誠鎬 主任研究員は、中部大学 工学部応用化学科 櫻井 誠 教授、大阪大学 大学院工学研究科 中野 貴由 教授、名古屋工業大学 春日 敏宏 名誉教授と共同で、抗菌性と骨形成促進機能を両立する生体材料向けガラス(以下「生体用ガラス」という)として、MgO-ZnO-P2O5-SiO2系ガラスを開発しました。
生体用ガラスは、体内に入れると骨や生体組織と直接結合する生体活性を示し、骨欠損の補填材や歯周病治療用の材料、知覚過敏ケア用の材料として実用化されています。生体用ガラスのうちリン酸塩を主成分とするリン酸塩ガラスは、多様な元素を導入可能であり、その元素を無機イオンとして溶出して細胞機能を活性化することができます。一方で、無機イオンの供給が過剰な場合には細胞機能を阻害する可能性があります。無機イオンのうち、亜鉛は、骨形成に関わる生体必須微量元素として、また抗菌性を示す元素として知られていますが、細胞に対して毒性を示す可能性があり、亜鉛イオンを活用した生体材料を開発する際には、その溶出挙動を厳密に制御する必要があります。
今回、ガラス網目構造を形成する構成要素として亜鉛を用い、その溶出量を制御して、優れた抗菌性と骨形成促進機能を両立するMgO-ZnO-P2O5-SiO2系ガラスを開発しました。従来のリン酸塩ガラスは、リン酸塩のPO4四面体同士が酸素の共有結合を介した長い鎖状構造の骨格を持ちますが、今回開発したガラスは、酸素の共有結合による長い鎖状構造を含まない独特なガラス網目構造を持っています。本研究成果は、亜鉛やその他の成分がガラスから溶出することで、骨形成に関連する遺伝子の発現量を向上させることができ、新たな生体適応材料の開発への貢献が期待できます。
なお、この研究成果の詳細は、2025年9月6日(中央ヨーロッパ時間)に「Advanced Healthcare Materials」に掲載されました。
生体材料とは、生体と直接接触して治療や修復、機能補助を目的として用いられる材料であり、1960年代から1970年代にかけて生体に埋植しても有害作用をもたらさない生体適合材料が開発され、1980年代からは生体活性材料と生体吸収性材料が主に研究されてきました。近年では細胞活性化による組織再生機能を持つ材料の開発が盛んになっています。中でも生体用ガラスは、生体と直接接触することで、細胞を活性化して骨形成を促進する作用がある無機イオンを溶出するため、骨欠損の補填材や歯科修復材などに利用されてきました。
生体用ガラスのうちリン酸塩を主成分とするリン酸塩ガラスは、窓ガラスなど汎用的に用いられるケイ酸塩ガラスと比べ、多様な元素を導入可能です。ガラスに取り込んだ無機成分は、無機イオンとして溶出しやすく、優れた細胞活性化機能を示します。しかし、その量が過剰な場合は細胞機能を阻害することもあります。そのため、細胞機能を活性化する無機成分およびリン酸塩ガラスを母材とした生体用ガラスを作製するには、ガラスから溶出する無機イオンの量を厳密に制御する必要があります。
産総研は、無機イオンによる細胞活性化機能を付与した生体用ガラスの創製に向けて、リン酸塩ガラスを母材とした生体用ガラスの開発を進めています。特に、導入する元素やガラス中での役割等を考慮してガラスの網目構造を適切に設計・制御することで、材料からのイオン溶出挙動を最適化した生体用ガラスの開発に取り組んでいます。
なお、本研究は日本学術振興会(JSPS)科研費(22K18201、23KK0272、24K22400)、二国間交流事業(120258813)、ガラス連合会およびニューガラスフォーラム ガラス研究振興プログラムの支援を受けています。
ガラスの骨格構造(ガラス網目構造)を形成する基本単位は、リン(P)やケイ素(Si)を中心に酸素(O)を4つの頂点とする、リン酸塩のPO4四面体やケイ酸塩のSiO4四面体であり、これらは網目形成成分と呼ばれます。一方、ナトリウム(Na)やカルシウム(Ca)などのアルカリ金属、アルカリ土類金属は、網目修飾成分と呼ばれ、リン酸塩やケイ酸塩の非架橋酸素に結合されます。
亜鉛(Zn)やマグネシウム(Mg)は、網目形成成分と網目修飾成分の両方の役割が可能ですが、制御せずにガラスに導入した場合には、ZnO6やMgO6の6配位構造となります。この構造はリンやケイ素より結合力が弱いので、ガラスの骨格構造を形成する網目形成成分とはならず、網目修飾成分として作用します。
今回開発したMgO-ZnO-P2O5-SiO2系ガラス(SPG-CZ/-MCZ/-MZ)は、亜鉛とマグネシウムが、ZnO4四面体、MgO4四面体の形で、PO4四面体やSiO4四面体をつなげる役割をします。一般に、リン酸塩やケイ酸塩といった網目形成成分同士がつながらない場合、非常に結晶化しやすく、ガラスを作ることはできません。リン酸塩とケイ酸塩がガラス網目構造中に共存するガラスは作ることが難しく、どちらかの成分が極端に多い場合のみガラスを得ることができます。また、リン酸塩ガラスは、ケイ酸塩ガラスと比べ少ない網目形成成分の組成(少ないP2O5含有量)でもガラス化します。開発したガラスは、PO4四面体やSiO4四面体が互いにつながることなく独立に存在し、その間をZnO4四面体やMgO4四面体がつなげた構造になるため、リン酸塩とケイ酸塩の両方がガラス網目構造中に多数共存した構造となっています。
開発したガラス中で、PO4四面体やSiO4四面体が、互いにつながることなく、単独で存在するオルト四面体であることは、31P、29Si固体核磁気共鳴分析(固体NMR)で確認しました(図1)。例えば、PO4四面体が2個つながった構造がある場合は、31P MAS-NMRのピークが-10 ppm付近に、PO4四面体がいくつかつながり鎖状構造を形成した場合は-20 ppm付近にピークが現れます。同じく、29Si MAS-NMRでも、SiO4四面体が2個つながった場合は-80 ppm付近に、鎖状構造になる場合は-85 ppm付近にピークが現れます。
今回は、亜鉛とマグネシウムに網目形成成分としての役割を担わせるため、ガラス骨格構造を形成するP2O5の含有量を極端に減少させ、PO4四面体が互いにつながりにくい組成に制御しています。その結果、特に亜鉛とマグネシウムが同時に導入されているSPG-MZとSPG-MCZガラスは、PO4、SiO4、MgO4、ZnO4のオルト四面体のみでガラス網目構造が形成されました。
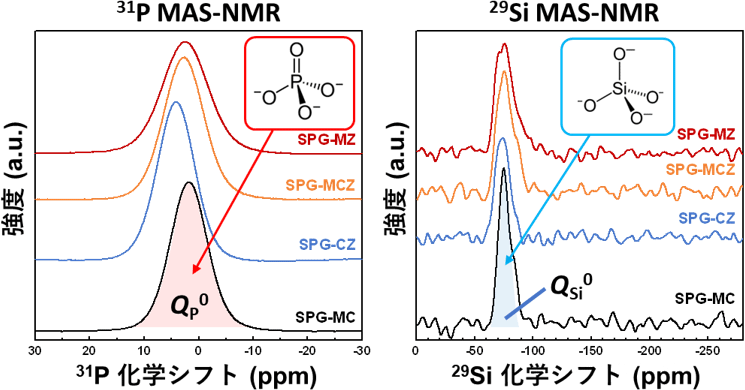
図1 開発したガラスの31P(左)、29Si(右)固体NMRのスペクトル。(SPG-MC: MgO-CaO-P2O5-SiO2ガラス(従来のオルト・ケイリン酸塩ガラス)、SPG-CZ: CaO-ZnO-P2O5-SiO2ガラス、SPG-MCZ: MgO-CaO-ZnO-P2O5-SiO2ガラス、SPG-MZ: MgO-ZnO-P2O5-SiO2ガラス)
※原論文の図を引用・改変したものを使用しています。
なお、ガラスに導入した亜鉛イオンは、優れた抗菌性・化学耐久性を発現させる利点がある一方で、生体中に過剰に溶出すると、細胞に対して毒性を示す場合もあります。このため、亜鉛を用いた生体材料を開発する際には、細胞に対して毒性を示さない範囲内に亜鉛イオン溶出量を制御する必要があります。今回開発したガラスに導入した亜鉛は、ZnO4四面体としてリン酸塩やケイ酸塩を強くつなぐガラス網目形成成分であることから、亜鉛を含めたガラス中の各種イオンの細胞中への溶出が、大きく抑えられています。亜鉛を含有しない従来のオルト・ケイリン酸塩ガラス(図2(a)SPG-MC)は7日までに約40%のイオンが溶出するのに対して、今回開発した亜鉛を適量含有しているガラス(図2(b-d)SPG-CZ/-MCZ/-MZ)は、ガラス中の各種イオンに対して浸漬時間7日間までで溶出率3%以下と通常のガラスに比べて10分の1以下に抑えることができました。開発したガラス(SPG-CZ/-MCZ/-MZ)の亜鉛イオンの溶出量は0.08 mM以下であり、細胞増殖性を50%阻害する濃度である0.1 mMより低い値を示しました。また、ヒト骨芽細胞の増殖性評価により、溶出した亜鉛イオンによって、細胞毒性を示さないことを確認しました。
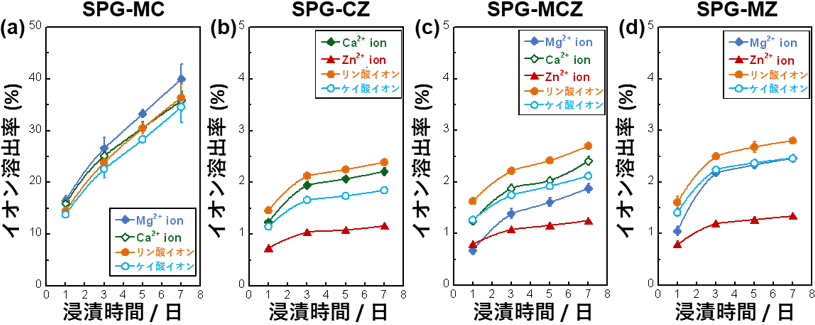
図2 開発したガラスをTris緩衝溶液(pH 7.4)に所定期間浸漬後のイオン溶出率。(SPG-MC: MgO-CaO-P2O5-SiO2ガラス(従来のオルト・ケイリン酸塩ガラス)、SPG-CZ: CaO-ZnO-P2O5-SiO2ガラス、SPG-MCZ: MgO-CaO-ZnO-P2O5-SiO2ガラス、SPG-MZ: MgO-ZnO-P2O5-SiO2ガラス)
※原論文の図を引用・改変したものを使用しています。
亜鉛イオンの抗菌性を確認するため、亜鉛含有ガラス存在下で、大腸菌、黄色ブドウ球菌をそれぞれ24時間培養した後の菌数を調べました(図3)。ガラスがなく菌のみで培養した場合の菌数(図中のControl)と比べ、2桁以上の菌数の減少が見られた場合に、抗菌性があると判断できます。亜鉛を含まないガラス(SPG-MC)はControlと同等の菌数を示しており、抗菌性がないことが分かります。一方、今回開発した亜鉛含有ガラス(SPG-CZ/-MCZ/-MZ)は、グラフ上では2桁以上の菌数減少に加え、装置でカウントできる下限(Blank: 細菌なしの培地のみで測定)に近い値を示していました。より詳細な菌数を求めるため、寒天培地上でのコロニー形成数をカウントした結果(図3 内表)、菌数を約6桁減少させる、優れた抗菌性を示しました。
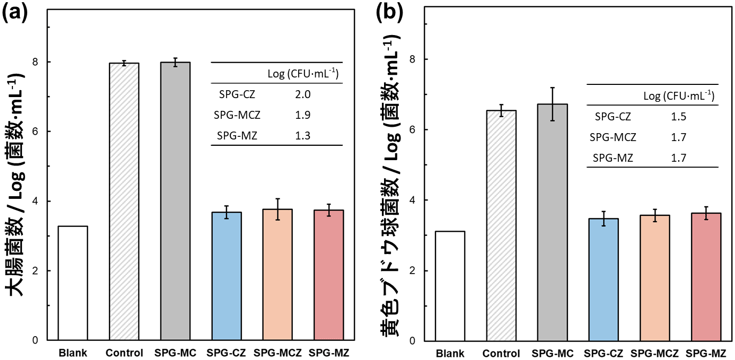
図3 開発したガラス(SPG-CZ/-MCZ/-MZ)と24時間培養後の(a)大腸菌、(b)黄色ブドウ球菌の数。内表:寒天培地を用いてカウントした菌の数。
(Blank:細菌なし、Control:細菌あり、サンプル名:細菌+各ガラスサンプル)
※原論文の図を引用・改変したものを使用しています。
骨形成促進機能についても調べました。骨芽細胞が骨を作るまでの各段階において、初期にはI型コラーゲン(Col I)、中期にはアルカリホスファターゼ(ALP)、オステオポンチン(OPN)、後期にはオステオカルシン(OCN)が代表的に発現する遺伝子であり、これら遺伝子の発現量を測定することで、骨形成の促進効果を評価することができます。一般に比較対象より1.5倍以上の値を示すと、遺伝子発現が促進されたと判断できます。開発したガラス(SPG-CZ/-MCZ/-MZ)から溶出するイオンを含有した培地で培養したヒト骨芽細胞は、すべての骨形成関連遺伝子において、Control(骨形成が早くなる骨形成分化誘導培地を使用)と比べ、中期のALPと後期のOCNに対しては50倍以上の遺伝子発現量を示していました(図4)。さらに、亜鉛を含有するガラスにおいては、亜鉛を含まないガラスと比べ優位に高い遺伝子発現量を示していました。特に、骨形成後期に発現するOCNは、亜鉛を含むガラスが含まないガラスと比べ約1.8倍高い遺伝子発現量を示しました。これらの結果は、開発したガラスが抗菌性と骨形成促進効果を両立することを示すものであり、導入した亜鉛が適度な濃度で溶出するような、ガラス網目構造が設計できたことを示しています。
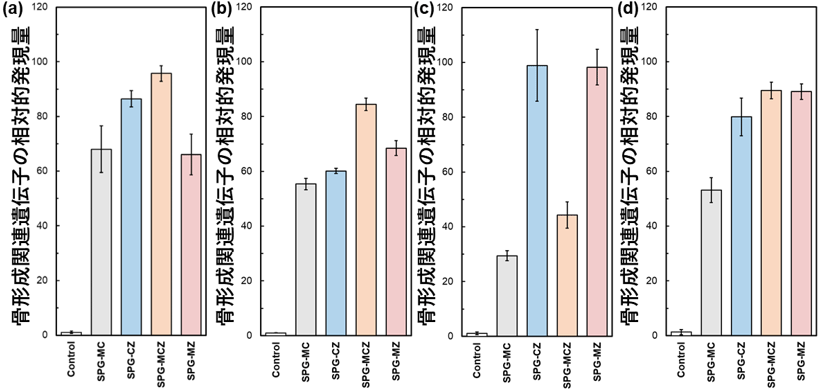
図4 開発したガラス(SPG-CZ/-MCZ/-MZ)より抽出したイオンを含有する細胞培養用培地を用いてヒト骨芽細胞を2週間培養後の骨形成関連遺伝子の相対的発現量。(a)I型コラーゲン(Col I)、(b)アルカリホスファターゼ(ALP)、(c)オステオポンチン (OPN)、(d)オステオカルシン(OCN)。
(Control:骨形成分化誘導培地、サンプル名:各ガラスから溶出した無機イオンを含有する培地)
※原論文の図を引用・改変したものを使用しています。
今後は、開発したガラスの抗菌性と骨形成促進効果を活用し、歯科用材料や組織工学に向けた細胞足場材料の開発を行います。
掲載誌:Advanced Healthcare Materials
タイトル:Preparation of Bifunctional Orthosilicophosphate MgO-CaO-ZnO-P2O5-SiO2 Glasses: in vitro Evaluation of Antibacterial Activity and Osteoblast Gene Expression Behavior
著者名:Sungho Lee*, Hayato Asano, Makoto Sakurai, Takayoshi Nakano, and Toshihiro Kasuga
DOI:10.1002/adhm.202502546