国立研究開発法人産業技術総合研究所(以下「産総研」という)モレキュラーバイオシステム研究部門 三浦 大典 主任研究員らと、国立大学法人九州大学 馬場 健史 教授ら、国立大学法人東京科学大学 難治疾患研究所 計算システム生物学分野 島村 徹平 教授、ブルカージャパン株式会社 韮澤 崇 博士らの研究グループは、イオンモビリティ(IM)分離技術を組み合わせたマトリックス支援レーザー脱離イオン化質量分析法(MALDI-MS)をヒト血漿に含まれる低分子量代謝物に適用することで、高速かつ再現性の高い分析手法を確立しました。この手法により複数のガン種における患者の層別化が可能であることを確認しました。
血液中に存在するアミノ酸や糖などの低分子量代謝物は、生活習慣や疾患などの影響を受けて変動するため、さまざまな遺伝的背景、病態を持つ多数の生体試料の低分子量代謝物をそれぞれ分析し、その情報を解析することで、健康状態や病態の特徴を明らかにできると期待されています。しかし、従来の低分子量代謝物の分析法は、測定の効率や再現性に課題があり、大規模(数千から数十万検体)の試料を同じ基準で分析することは困難でした。
今回、アセトニトリルで希釈するだけという極めて簡便な前処理と、IM分離技術を組み合わせたMALDI-MSを用いた低分子量代謝物の分析手法を確立しました。1検体あたり1秒以下と高速ながら、質量電荷比(m/z)およびイオン移動度の二軸で再現性の高い分析結果が得られます。また、この手法によって得られる血液中の複数の代謝物情報から、健常人と胃ガンや大腸ガンなど複数のガン種の患者を区別して層別化できることを確認しました。
低分子量代謝物を体系的に解析するメタボロミクスでは、バイオバンクに蓄積された多様なヒト試料からビッグデータを構築し、疾患の指標となる代謝物(バイオマーカー)の探索や精密医療に向けた基盤を整備することが期待されています。今回開発した手法は、こうした取り組みを加速するための重要な成果です。
なお、この研究成果の詳細は、2026年3月9日に「Microchemical Journal」に掲載されました。
血液や尿などの生体試料には、体内の代謝過程で生成・変化するアミノ酸や糖といった低分子量代謝物が含まれています。これらの代謝物は、遺伝的背景に加え、生活習慣、疾患、薬剤などの影響を受けて変動するため、その種類や量を調べることで、個人の健康状態や病態を反映する重要な情報が得られると考えられています。
低分子量代謝物を網羅的に測定し、生体の状態を分子レベルで理解する研究分野はメタボロミクスと呼ばれています。メタボロミクスでは、近年、国内外のバイオバンクに蓄積された多様なヒト試料を解析し、ビッグデータとして統合することが期待されています。こうして構築されたビッグデータから、特定の疾患や病態によって変動する代謝物を見いだすことができれば、診断や治療標的の探索に役立つ指標、すなわちバイオマーカーの発見や、患者個人の特徴に合わせた治療を選択する精密医療の基盤となる可能性があります。
これまで、低分子量代謝物の解析には、主にクロマトグラフィー分離と質量分析を組み合わせた手法が用いられてきました。しかし、前処理に多くの工程と時間を要し、測定自体にも1検体あたり数十分を必要とします。また、測定条件や装置状態のわずかな違いによって解析結果が変動しやすく、長期間にわたって整合性の高いデータを大量に蓄積することが難しい、という問題がありました。
一方、質量分析にはクロマトグラフィーを用いずに高速測定できる方式もあり、その1つがMALDI-MSです。これは、試料にマトリックスと呼ばれる化合物を加えてレーザーを照射し、イオン化した分子を真空中に飛ばして質量を測定する方法で、もともとタンパク質などの高分子量の化合物を対象に広く利用されてきました。しかし、低分子量代謝物の分析では、イオン化を妨げる塩やタンパク質を事前に試料から除去する必要があるほか、マトリックス自体が目的の代謝物と干渉してしまうことから、適用が難しいと考えられてきました。
産総研では、MALDI-MSを低分子量代謝物の分析に応用するため、干渉の少ないマトリックスの探索や分析条件の最適化に取り組んできました。今回、全身の臓器や組織からの代謝情報を含んでいるヒト血漿を対象に、簡便な前処理と高速分析技術の開発に取り組みました。
なお、本研究は日本学術振興会 科学研究費助成事業 基盤研究(B)(20H02872、代表:三浦大典)の助成を受けたものです。
医療や創薬の分野では、血液中に含まれる「代謝物」と呼ばれる小さな分子を調べることで、疾患の兆候を早期に見つけたり、患者ごとに最適な治療を選んだりする「精密医療」が進みつつあります。しかし、従来の分析方法では1つのサンプルを調べるのに数分~数十分かかり、バイオバンクのような数千から数万規模の大規模調査には膨大な時間と労力がかかるという問題がありました。本研究では、この問題を解決するために、血液サンプルを「1秒以内で」分析できる新しい超高速メタボロミクス技術を開発しました。
まず本研究で取り組んだのは、「どのようにすれば短時間で多くの代謝物を正確に測定できるか」という課題です。そこで本研究グループは、レーザーを利用してサンプル中の分子を一気に気化・イオン化するMALDI-MSと、気体中で分子の形や大きさを識別するイオンモビリティ(IM)分離を組み合わせました。この2つの技術を統合することで、従来では重なって区別できなかった代謝物同士を、質量電荷比(m/z)とイオン移動度という2つの情報で分離できます。
次に、「誰でも再現良く測れる簡単な前処理」を実現するため、血液の液体成分である血漿をアセトニトリルで薄めるだけの単純な抽出法を導入しました。これにより塩とタンパク質が取り除かれ、代謝物が効率よく検出できるようになります。複雑な操作が不要なため、ロボットによる自動化とも相性が良く、大規模測定に向いた方法です。
開発した測定系を使うと、1サンプルの分析時間はわずか1秒以下となり、一度の測定でヒトの血漿から約1,000種類もの代謝物由来のシグナルを安定して検出できました。測定の再現性も高く、サンプル内の複数箇所から得られるシグナルを平均化することでばらつき(CV)は20 %未満に抑えられています(図1A)。また、クロマトグラフィー分離を行わないMALDIでは個別に検出することが難しいとされる「同重体(質量は同じだが形の違う分子)」も、イオンモビリティにより明確に区別できるようになりました(図1B)。
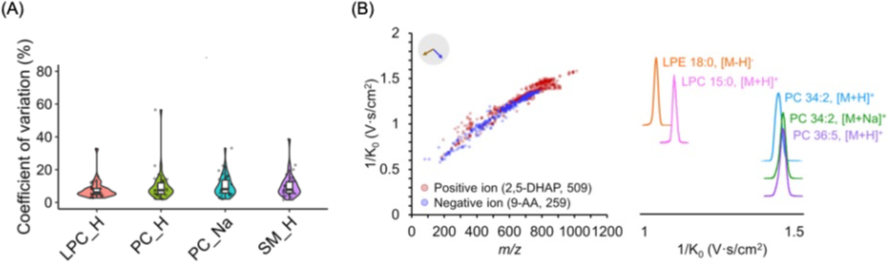
図1 (A)代表的な脂質について、34検体を繰り返し測定した際の変動係数。(B)IM分離技術を組み合わせたMALDI-MSで検出されたピークのm/zとイオン移動度の関係(陽イオンは赤、陰イオンは青)。右パネルは同重体(異性体および同位体脂質)の移動度プロファイルを示す。同重体をイオン移動度によって分離できている。
※原論文の図を引用・改変したものを使用しています。
さらに本研究では、この超高速測定が実際の疾患の違いを捉えられるかを確かめるため、健常人と4種類のガン患者の血漿を解析しました。その結果、34検体という小規模ながら、データを圧縮表示するUMAPと呼ばれる手法で、ガン種ごとの代謝物パターンの違いが明確に表れました(図2)。UMAPは高次元データを2次元に圧縮して表示する手法であるため、一部の検体では異なる群が近接して表示される場合もありますが、各患者由来のデータは全体として疾患ごとに異なる分布傾向を示していました。特に、ガン患者血漿で濃度が低下することが知られる「リゾホスファチジルコリン(LPC)」が、本研究のデータでも同様に低下しており、実臨床で見られる変化を正しく捉えられることが確認できました。
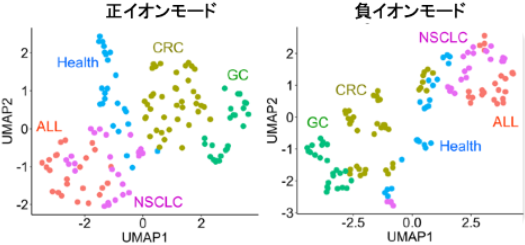
図2 正イオンモードと負イオンモードの両方で取得した34検体のUMAPプロット。両極性において、健常人(Health)、急性リンパ性白血病(ALL)、非小細胞肺ガン(NSCLC)、大腸ガン(CRC)、胃ガン(GC)の層別化が可能。
※原論文の図を引用・改変したものを使用しています。
以上の結果は、本技術が数千から数万検体規模の臨床研究やバイオバンク解析を現実的にする「次世代メタボロミクス基盤」となり得ることを示しています。血液1滴から疾患に伴う代謝の変化を素早く捉え、精密医療の実現を支える技術として、ビッグデータ生成法としての有用性検証を進めます。
今回開発した分析技術は血中成分の迅速分析に限らず、食品・農作物中成分の迅速評価や微生物の発酵過程モニタリング、環境サンプルの分析など幅広い分野への応用が期待されます。
掲載誌:Microchemical Journal
タイトル:Ultrahigh-throughput metabolomics for large-scale studies using matrix-assisted laser desorption/ionization-ion mobility-mass spectrometry
著者名:Hiroaki Takeda, Daisuke Miura*, Teppei Shimamura, Yoshinori Fujimura, Masatomo Takahashi, Mitsuru Shindo, Ryo Nakabayashi, Takashi Nirasawa, and Takeshi Bamba*
DOI:10.1016/j.microc.2026.117523
産総研
モレキュラーバイオシステム研究部門 三浦 大典 主任研究員、竹田 浩章 産総研特別研究員
九州大学
生体防御医学研究所 馬場 健史 教授、髙橋 政友 助教
大学院農学研究院 藤村 由紀 准教授
先導物質化学研究所 新藤 充 教授
東京科学大学
総合研究院 難治疾患研究所 計算システム生物学分野 島村 徹平 教授
ブルカージャパン株式会社
アプリケーション部 中林 亮、韮澤 崇