独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)ユビキタスエネルギー研究部門【研究部門長 小黒 啓介】ナノ材料科学研究グループ【研究グループ長 香山 正憲】吉川 純 産総研特別研究員、秋田 知樹 主任研究員らは、リチウムイオン電池の正極でのリチウムイオンの出入りの様子をナノメートルスケールで可視化する電子顕微鏡技術を開発した。
自動車への利用に向けてリチウムイオン電池を高性能化するためには、電池正極材料でのリチウムイオンの出入りの様子を明らかにする必要がある。STEM-EELSスペクトラム・イメージング法は、試料の構成元素の濃度分布を可視化できる電子顕微鏡技術であるが、リチウムは軽元素であるため、これまで可視化は困難であった。今回、独自のスペクトルデータ処理法を開発しリチウムの濃度分布の可視化に成功した。この技術を用いて、正極材料のナノ構造とリチウムイオンの挙動の関係を解明した。今後、ナノメートルレベルで微細構造を設計・制御した新規正極材料の開発に貢献できると期待される。
本研究は、独立行政法人 新エネルギー・産業技術総合開発機構(NEDO)の委託研究「次世代自動車用高性能蓄電システム技術開発(Li-EADプロジェクト)-高容量・低コスト新規酸化物正極材料の研究開発-」の支援を受けて行った。本成果は、Electrochemical and Solid-State Letters(米国電気化学会)電子版に2008年8月15日掲載された。
|
|
|
|
図1 リチウムイオン電池の正極材料(Li2MnO3-LiFeO2)のリチウム元素濃度分布(左)と遷移金属元素濃度分布(右)。
リチウム元素濃度は青→緑→赤→黄の順に上がる。遷移金属濃度分布は、黄色が鉄を含むLiFeO2ドメイン(右図B’)、緑・青がマンガンを含むLi2MnO3ドメイン(右図A’)。50%充電時(充電は正極材料からリチウムを抜く過程)のもので、LiFeO2ドメイン(左図B)からリチウムが抜けているが、Li2MnO3ドメイン(左図A)にはリチウムが残っている。
|
リチウムイオン電池は、軽量で容量が大きく、繰り返し使えることから、携帯電話やノートPCに広く普及している。さらに高性能になれば、電気自動車やプラグインハイブリッド車の電源として利用できるようになる。家庭で夜間に充電した電気で走行するこれら自動車は、CO2や排気ガスの大幅な低減が可能であり、その実現が望まれている。
リチウムイオン電池の動作原理は図2のように、充電時に正極材料(リチウム遷移金属酸化物など)からリチウムイオンが脱離し、電解液中を拡散して負極材料(グラファイトなど)内へ挿入される(電子は負極側へ移動)。放電時には逆に負極側から正極側へリチウムイオンが戻る。正極材料からどのくらいリチウムイオンが取り出せるかで容量が決まり、正極材料での脱離・挿入時の電圧が電池の電圧を決定づける。
新たなリチウムイオン電池の正極材料として、複数の遷移金属化合物を複合化した材料への期待が高まっている。正極材料のさらなる高性能化のためには、複合化したナノスケールの微細構造でのリチウムイオンの出入りの様子を観察することが重要である。しかし、リチウムのような軽元素を電子顕微鏡で観察することは原理的に難しいことから、リチウムイオンの挙動を可視化できる電子顕微鏡観察技術の開発が望まれていた。
産総研では、これまで、従来のコバルトを用いた正極材料に比べて、安価で資源の豊富なマンガンや鉄、チタン等を用いた正極材料の開発に取り組み、従来の材料を超える高容量の正極材料の開発に成功した(プレス発表 2006年11月6日)。
このような複数の遷移金属化合物からなる正極材料の高容量化のメカニズムを解明するために、Li
2MnO
3-LiFeO
2(> 200 mAh/gの高容量)について、電子顕微鏡による観察を試みてきた。
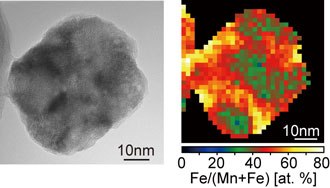
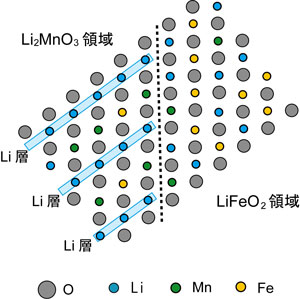
今回、可視化の対象とした材料は、Li2MnO3-LiFeO2である(Li1.2Mn0.4Fe0.4O2、鉄含有リチウムマンガン酸化物)。この材料の各粒子では、Li2MnO3とLiFeO2の二つの酸化物結晶が、ナノメートルサイズのドメイン(領域)を形成しているが、酸素は両ドメインに共通の格子を形成しており、特異なナノ構造体であることが電子顕微鏡観察により判明した(図3)。図3(b)に示すように、粒子内には、マンガンが高濃度のドメイン(緑・青)、鉄が高濃度のドメイン(黄色)がある。図3(c)のように、各々、Li2MnO3に近い組成のドメインとLiFeO2に近い組成のドメインである。
(a )(b)
|
(c) |
|
図3 高容量の正極材料Li2MnO3-LiFeO2粒子の透過電子顕微鏡像(a)、STEM-EELSスペクトラム・イメージング法による遷移金属元素濃度分布(b)、化学ナノドメイン構造の概念(c)。 |
このような化学ナノドメイン構造が、高容量を生みだすメカニズムを解明するには、遷移金属濃度分布だけではなく、リチウム元素分布を観察し、充電・放電過程でのリチウムイオンの挙動を観測することが必要である。STEM-EELSスペクトラム・イメージング法は、図3で遷移金属濃度を分析したように、元素濃度分布を定量化、可視化するのに有効である。しかし、リチウムについては、スペクトルのピークがエネルギー的に低い位置にあるため、バックグラウンドや他元素のピークと混成し、定量的な信号強度解析が容易でなく、濃度分布の可視化は困難であった。
今回、試料が薄い場合、EELSスペクトルの2階微分値が理論的に濃度に比例する事実を見出し、2階微分値を用いた信号強度解析法を独自に開発することで、リチウムによる信号強度を定量化し、濃度分布を可視化することに成功した。図4(図1)に示すように、実際の充電、放電の各過程で取り出した試料粒子について、遷移金属元素濃度分布図とリチウム元素濃度分布図の両方を観測できるようになり、各過程でのリチウムイオン挙動を明らかにできた。
|
|
|
図4 リチウムイオン電池の正極材料(Li2MnO3-LiFeO2)の粒子の、充電・放電の各過程
(左から右、(i)~(iv))での、遷移金属元素濃度分布図(上図)とリチウム元素濃度分布図(下図)。
|
(i)の充電前の試料では、粒子はLi2MnO3(緑・青)とLiFeO2(黄)の化学ナノドメイン構造となっている(上図)。この段階ではリチウムイオンは、粒子全体に分布していることがわかる(下図)。
(ii)の50%充電の試料では、リチウム元素濃度分布の青の領域(下図)と遷移金属濃度分布の黄色の領域(上図)とが一致していて、充電初期にはリチウムイオンはLiFeO2ドメインから優先的に脱離している。
(iii)の100%充電の試料では、粒子全体(Li2MnO3とLiFeO2の全ドメイン)からリチウムイオンが脱離している(下図)。
(iv)は放電後の試料の元素濃度分布であるが、粒子全体にリチウムイオンが戻っている(下図)。しかしながら、リチウムイオンの分布にむらがあり、リチウムが粒子全体に充分には戻っていない。
これらの観察から以下の点が明らかとなった。(1)Li2MnO3とLiFeO2の各化合物は、単独ではリチウムイオンの出し入れは起こらず正極として使用できないが、ナノドメイン構造をとることでリチウムの出し入れが起きるようになる。(2)性質の異なるLiFeO2とLi2MnO3とが、複合化したナノドメイン構造になることで、各々の利点(LiFeO2はリチウムイオンが比較的取り出しやすい。一方、Li2MnO3は層状構造であるためリチウムイオンが移動しやすく、また多くのリチウムイオンを取り込めるため、高容量化に寄与する)が発揮されて、高性能化につながっていると推定される。(3)Li2MnO3からも確実にリチウムイオンが抜けていることが初めて明確に観測された。マンガンイオンは価数が変化しないので、酸素が電荷補償を担うと推定される。(4)従って、容量の低下や劣化には、酸素の離脱が関係する。
今回、独自のスペクトルデータ処理法を開発しリチウムの濃度分布の可視化に成功した。この技術を用いて、正極材料のナノ構造とリチウムイオンの挙動の関係を解明した。
この手法により得られた、化学ナノドメイン構造による材料設計の指針をもとに、正極材料のナノ構造化・複合化を進めて、高性能正極材料を開発していく。また、さらに観測手法の改良を重ねるとともに、様々な新規材料への適用を進める計画である。