独立行政法人 産業技術総合研究所【理事長 吉川 弘之】(以下「産総研」という)生物機能工学研究部門【部門長 巌倉 正寛】の富田 耕造 研究グループ長と独立行政法人 科学技術振興機構【理事長 沖村 憲樹】の濡木 理 研究員(東京工業大学 教授)らは鋳型なしでRNAを合成する特殊なRNA合成酵素の反応機構の全貌を明らかにした。
細胞内でタンパク質が合成される際、アミノ酸を運んでくるtRNAという70-90塩基のRNA1本鎖があり、このRNA鎖の大部分はDNAを鋳型として合成されるが、tRNA末端にある3つの塩基配列CCAだけはCCA付加酵素というRNA合成酵素によって合成される。この酵素は鋳型なしで塩基配列CCAを合成するユニークな酵素であるが、そのメカニズムは謎であった。
本研究は鋳型なしでRNA塩基配列を合成する酵素の全反応機構を世界ではじめて明らかにしたものである。これにより、鋳型なしで特定の塩基配列を合成できるRNA合成酵素の設計・開発、機能性タンパク質開発が可能になると期待される。
本研究成果は、平成18年10月15日に、英国科学誌 Nature 電子版に掲載される。
DNAの遺伝情報はRNAへ転写され、その後タンパク質へと翻訳される。長年RNAは単なるDNAのコピーであり単に情報伝達の一時的ななかだちにすぎないと考えられてきた。しかしながら、近年RNA 干渉等、RNAが生体において遺伝子発現の制御に積極的に関与していること、さらにその制御が高次生命現象の発現に深く関わっていることがあきらかになってきた。RNAの機能解析、機能性RNA分子の生合成の機構解明は重要な課題となりつつある。
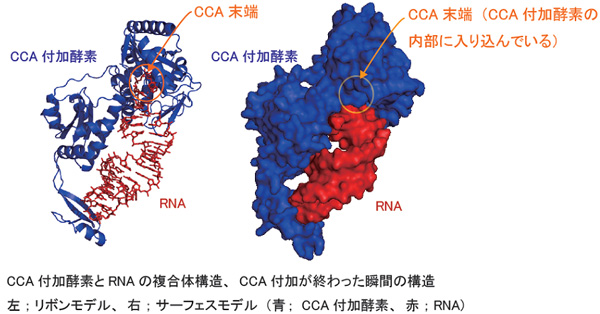
細胞内でタンパク質が合成される際において、tRNA(転移RNA)はアミノ酸の運び屋として働いているRNA1本鎖であり、常時30種から40種のtRNAが細胞内で働いている。全てのtRNAの3'末端にはCCAという配列が存在し、その末端塩基Aにアミノ酸が結合して、必要とされる場所にアミノ酸が運ばれる。tRNA本体の70-90塩基のRNA鎖はDNAを鋳型として合成されるが、末端のCCA配列だけはCCA付加酵素とよばれる鋳型非依存性RNA合成酵素によって合成される。
CCA付加酵素は全生物に保存されている酵素であり、鋳型となるDNAやRNAなしできまった塩基配列を合成できるユニークな酵素である。これまで、鋳型非依存性RNA合成酵素の反応機構に関しては30年以上謎であった。
産総研は、生体内において機能をもったRNAが生成されるまでのプロセス(成熟化プロセス)およびRNAの品質管理システムの分子機構、機能と構造の相関に関する研究を推進している。
本研究では機能をもったtRNAの成熟化プロセスに関与する鋳型非依存性RNA合成酵素の動的反応機構の全貌解明を目指して、X線結晶構造解析、生化学的解析の両方を用いて解析を行なった。
DNAやRNAの鋳型を用いずにきまった塩基配列のRNAを合成する酵素の分子基盤を明らかにすることを目指して、酵素とRNA鎖の会合、塩基単量体(ヌクレオチド)の会合、鎖伸長、終結反応に相当する酵素、RNA鎖、ヌクレオチド複合体のX線結晶構造解析を行なった。
表に示すようにCCA酵素と4種類のRNA鎖の二者複合体、CCA酵素と二種類のRNA鎖および塩基単量体の三者複合体、計6種類の複合体の構造決定を行なった。
その結果(図1)、「酵素-RNA鎖」の二者複合体(構造決定1、2)では、酵素は「開いた」構造をとっており、RNA鎖の3'末端は酵素の活性触媒部位から離れているので仮に活性触媒部位へC塩基単量体がきても付加反応ができない「不活性型」であった。ところが、その二者複合体へC塩基単量体を加えた「酵素-RNA鎖-C塩基単量体」の三者複合体(構造決定3)では、酵素は「開いた」構造から「閉じた」構造へと変化しており、それに伴い、RNA鎖の3'末端が「ひっくり返り」C塩基単量体の付加反応が進行できるように酵素は「活性型」へ移行していた(図1[1])。一方、最後のA塩基単量体の付加反応においては、「酵素-RNA鎖-C-C」の二者複合体(構造決定4)ですでにRNA鎖の3'末端は活性触媒部位から近いところに位置し、酵素はすでに「閉じた」「活性型」の構造をとっていた。また、活性触媒部位のポケットの形と大きさはA塩基単量体に適したものになっており、A塩基単量体がやってくればそのまま付加反応が進行する状態であることがわかった(図1[2])。
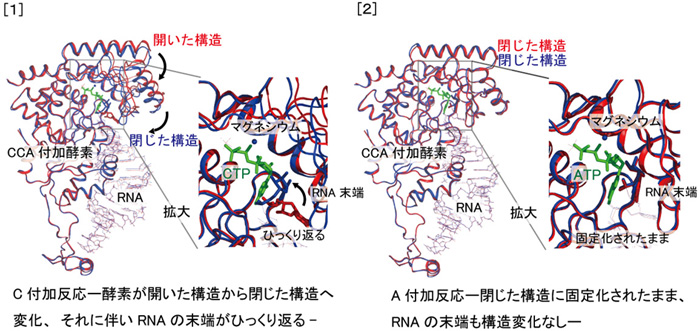 |
図1 [1] 赤:構造解析2及び青:構造解析3
緑CTP:C塩基単量体 |
[2] 赤:構造解析4及び青:構造解析5
緑ATP:A塩基単量体 |
これらの結果から、鋳型非依存性CCA酵素の反応機構は次のように説明できる。
1)C塩基の付加反応においては酵素-RNA鎖複合体に、C塩基単量体が酵素触媒部位に結合すると、酵素とRNAの複合体の「動的」な変形が誘発され、RNA鎖末端にC塩基単量体の付加が行われる。
2)最後のA塩基の付加反応においては、酵素にRNA鎖-C-Cのみが結合した「静的」な状態のままでA塩基の付加が行われ、反応が終結する、といったユニークな分子機構であることが明らかになった。
本研究は、鋳型非依存的なRNA合成反応の開始、鎖伸長、終結の際の酵素とRNA鎖の動的変化を世界ではじめて詳細に解明したものであり、この研究結果により、過去に詳細に研究されてきた鋳型依存性RNA/DNA合成酵素の動的反応機構と比較が可能になり、他の鋳型非依存性RNA合成酵素の動的反応機構研究の基礎となるものである。これにより、鋳型を用いずに目的の配列をもったRNAを合成する酵素開発が可能になる。また、非天然型アミノ酸の運び屋tRNAの開発やそれに基づいた機能性タンパク質開発も期待され、医薬や新しい治療方法へ応用も期待される。