独立行政法人 産業技術総合研究所【理事長 吉川 弘之】ナノテクノロジー研究部門【部門長 横山 浩】(以下「産総研・ナノテク部門」という)の 山嵜 登 主任研究員 と 大阪大学【総長 宮原 秀夫】医学部眼科学教室【教授 田野 保雄】(以下「阪大・医学部」という)の 大黒 伸行 講師 らのグループは、世界で初めて、炎症性疾患治療用アクティブ・ターゲティングを可能にする糖鎖導入型のDDSナノ粒子を作製し、そして、炎症性疾患モデルとしての眼炎症モデルマウスを作成して、この標的指向性DDSナノ粒子が炎症疾患組織へ標的分子としてのレクチンを利用して疾患部位選択的にアクティブ・ターゲティングされることを実証した。
従来、アクティブ・ターゲティング用の各種リガンド(抗体、ペプチド、糖質など)を結合したリポソームなどのDDSナノ材料について多くの研究がなされてきた。しかしながら、それらは、生体外では標的細胞に結合しても、生体内では期待される標的細胞や組織にターゲティングされないものがほとんどであった。本成果は、産総研・ナノテク部門の開発した糖鎖導入型のアクティブ標的指向性DDSナノ粒子の作製技術と、阪大・医学部が開発した炎症性疾患組織の標的分子へのアクティブ・ターゲティング機能解析技術とを融合することにより達成したものであり、本技術開発によって、炎症性疾患全般(脳炎、網脈絡膜炎、肺炎、肝炎、関節炎など)、並びに、続発的に炎症を引き起こす疾患(悪性腫瘍、リウマチ、脳梗塞、糖尿病、アルツハイマー病など)の治療に応用可能なDDS製剤開発を加速するものである。
今後は、本技術を癌治療、遺伝子治療、再生医療などの各分野での新しい治療を実現させるために必要なデリバリーシステムの開発・実用化へと展開する予定である。
DDSは Drug Delivery System の略称で薬物送達システムと訳されている。その中でも標的指向(ターゲティング)DDSとは、癌など各種疾患部位の標的細胞・組織を認識し局所的に薬剤や遺伝子を送り込むためのシステムである。この分野での現在の開発動向は、パッシブ・ターゲティング(受動的・標的指向性)DDSナノ材料が販売あるいは開発されつつある状況である。一方、高機能のターゲティングを可能にするためのアクティブ・ターゲティング(能動的・標的指向性)DDSはミサイルドラッグとも呼ばれ、21世紀の夢のターゲティングDDSとして大いに期待されている。
高齢化社会になるに従い癌の罹患率・死亡率は年々増えており、新規な治療用ナノ材料である標的指向性DDSの開発が待望されている。その他の病気においても副作用のないアクティブ標的指向性DDSナノ材料技術開発の重要性が注目されており、その市場規模は将来10兆円を超えるとの予測もある。本技術を確立・発展させることにより、癌や炎症性疾患など各種疾患患部の標的細胞や組織を認識し、局所的に薬剤や遺伝子を患部に送り込むための治療用のドラッグデリバリーシステムや診断用の細胞・組織センシングプローブとして利用できる標的指向性ナノ粒子の創製技術など、これら市場規模の大きな医療分野でのナノテク応用新規産業への迅速な参入と国際競争力の強化を図ることができる。
本研究では、核酸、蛋白質に次ぐ第三の鎖として現在のライフサイエンスで注目されている糖鎖のかかわる分子・細胞認識機能に着目して、新規な分子認識素子としての糖鎖導入型の高機能な標的指向性DDSナノ材料の合成技術の基盤整備を目指してきた。そして、糖鎖構造の異なる多種多様な糖鎖導入型DDSナノ粒子を合成してそれらの分子認識や体内動態を調べることにより、これらの新規なDDSナノ材料構築のための基本技術の確立を図っている。そして、これらの新規DDSナノ粒子の生体内における機能解明や新規治療用製剤開発など実用化へ向けての研究を阪大・医学部との協力により推進している。
(1) アクティブ標的指向性DDSナノ粒子の作製技術
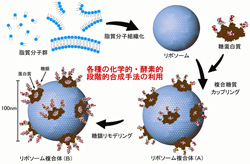
本技術の課題は、生体内で各種組織の細胞表面上に存在する各種のレクチン(糖鎖認識蛋白質)に対して特異的な結合活性を有する糖鎖を導入したリポソームであって、実際の生体内の細胞、組織を識別して薬剤あるいは遺伝子を効率的に輸送し得るリポソームを提供することにある。この課題を解決するために、本研究者らは、リポソーム表面の性質あるいは該表面に結合させる糖鎖およびリンカー蛋白質について種々の実験、検討を加え、該結合糖鎖分子の構造設計により各組織への標的指向性を実際に制御できることを見いだし本技術を完成するに至ったものである。【図1】
|
|
|
図1 新規DDSナノ粒子の作製方法の一例
※図をクリックすると拡大図が表示されます
|
(2) 炎症性疾患組織の標的分子によるアクティブ・ターゲティング機能の解明
本研究では、炎症性疾患部位の標的組織に集積し、局所的に薬剤や遺伝子を患部に送り込むための治療または診断用のDDSとして利用できるアクティブ標的指向性DDSナノ粒子の機能解析を行った。具体的には、炎症性疾患部位の血管内皮細胞に発現する複数の標的分子と特異的に結合しうる糖鎖を導入したリポソームの炎症性疾患組織への標的指向性機能の解明を目指した。この課題を解決するために、本研究者は、この標的指向性リポソームの炎症性疾患領域への応用について鋭意検討を行い、炎症性疾患モデル動物として眼炎症モデルマウスを作成し、上記標的指向性リポソームが眼の炎症部位に選択的に取り込まれることを見出し本技術を完成するに至ったものである。【図2、図3、図4】
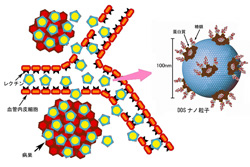
図2 アクティブ・ターゲティング機能の模式図
※図をクリックすると拡大図が表示されます
|
|
 |
|
|
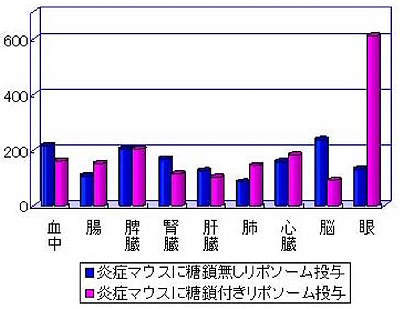
図3 炎症モデルマウスの炎症性疾患組織(この場合は眼炎症部位)へのDDSナノ粒子の選択的組織分布を示す図(各臓器分布の正常マウスに対する相対値%で表示、尾静注30分後)
|
 |
|
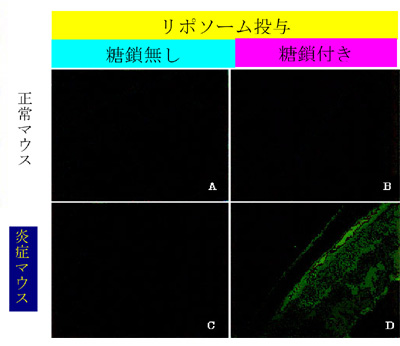
図4 炎症モデルマウスの眼炎症部位の網膜及び脈絡膜細胞へのDDSナノ粒子のアクティブ・ターゲティング(写真D)を示す蛍光顕微鏡写真
|
基本特許は既に出願済みであり、今後は実用化に向けて、本技術をコアとするコンソーシアムを設立して、医薬品メーカーとの共同研究による産学官の連携を強化していく予定である。