国立研究開発法人 産業技術総合研究所【理事長 中鉢 良治】(以下「産総研」という)バイオメディカル研究部門【研究部門長 近江谷 克裕】脳遺伝子研究グループ 落石 知世 主任研究員らは、国立大学法人 北海道大学【総長 山口 佳三】大学院 先端生命科学研究院 北村 朗 助教、学校法人 順天堂【理事長 小川 秀興】 順天堂大学 医学部 脳神経内科 志村 秀樹 准教授らと共同で、アルツハイマー病の原因因子の一つであるアミロイドβ(Aβ)タンパク質の動態を、生きた神経細胞内や生体内で可視化する技術を開発した。
Aβは容易に重合し、それが更に集まって大きな凝集体を形成する。Aβと蛍光タンパク質のGFPを融合させたタンパク質(Aβ-GFP)は、Aβの重合によりGFPの蛍光が阻害されると推測されている。そのため、生体内で発現させてもAβが重合すると蛍光が観察されず、これまでAβの局在や動態を可視化することは困難であった。今回、AβとGFPを繋ぐアミノ酸配列(リンカー)を工夫することで、Aβの重合状態に関係なくGFPの蛍光が観察できる融合タンパク質を開発した。また、この融合タンパク質はアルツハイマー病の発症に関与する毒性の強いAβオリゴマーを形成することが分かった。
この技術は、培養細胞や生きた個体を用いたアルツハイマー病治療薬の候補物質のスクリーニングへの応用や、アルツハイマー病の発症メカニズムの解明への貢献が期待される。なお、本成果の詳細は、2016年3月16日にScientific Reports誌(電子版、オープンアクセス)に掲載される。
 |
|
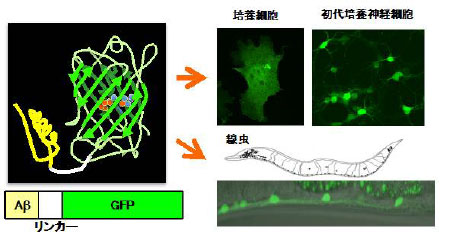
開発したAβ-GFP融合タンパク質の模式図(左)と、培養細胞や線虫内での発現の様子(右) |
高齢化社会を背景とした認知症患者の増加は、医療費や介護制度の現状などが絡み合い、世界的にも大きな社会問題となっている。特にアルツハイマー病は記憶障害や判断能力の低下、見当識障害等を特徴とし、認知症の半数以上を占めるにもかかわらず、詳細な発症メカニズムが解明されておらず、有効な治療法や特効薬も開発されていない。
産総研では、生体メカニズムや疾病に関連する分子の機能・構造の解明を目指した研究を推進しており、そこから得られた知見を基に創薬基盤・医療基盤技術の開発に取り組んできた。アルツハイマー病は、Aβを主成分とする老人斑の神経細胞周囲への沈着と、過剰にリン酸化されたタウタンパク質が神経細胞内に蓄積する神経原繊維変化および、脳の萎縮を主な病理学的特徴とする認知症である。これらは発症原因として有力であるものの、いまだアルツハイマー病発症のメカニズムは解明できていない。このような背景の中で、最近少数のAβ分子が重合したAβオリゴマーが細胞に対する強い毒性を有し、これが細胞内に蓄積されることが病気の発症に強く関与するという説が有力になりつつある。しかし従来の方法では、細胞や脳組織の標本を用いた解析しかできなかったため、生きた細胞内でAβのオリゴマー化の状態を直接可視化して毒性との因果関係を詳細に解析する方法や、治療薬の候補となる物質のAβの重合に対する効果を直接解析する新たな手法が求められていた。そこで、細胞の可視化や、神経細胞の機能の解析、トランスジェニック動物の作成と解析を行っている産総研と、生きた細胞内での分子の相互作用を解析する蛍光相関分光法に優れた実績を持っている北海道大学大学院先端生命科学研究院で共同研究を行うこととした。
これまで、AβとGFPを繋ぐリンカーとして12個以下のアミノ酸から構成されたものが報告されていたが、これらはAβが重合するとGFPの蛍光が消失するため、毒性の強いオリゴマーを観察できていなかった。今回、AβとGFPを繋ぐリンカーとして、14個のアミノ酸を用いて、Aβ分子の重合体が形成されても蛍光を観察できる、Aβ-GFP融合タンパク質(Aβ-GFP)を開発した。このAβ-GFPを核磁気共鳴装置や電子顕微鏡、免疫組織化学法、蛍光相関分光法で解析したところ、GFPを融合させたことでAβの重合が一定以上進まず、生体内でも生体外でも2量体から4量体を中心としたオリゴマーの状態で存在することが分かった(図1)。これらの特徴を活かし、生きた細胞内でAβのダイナミックな動きや、初代培養神経細胞内での蓄積状態などの解析が可能となる。また、重合が進んで繊維状となったAβよりも、オリゴマーのほうがより強い毒性を有することから、Aβオリゴマーの重合の度合いと細胞への毒性との関係などの解析を行うことができる。
 |
|
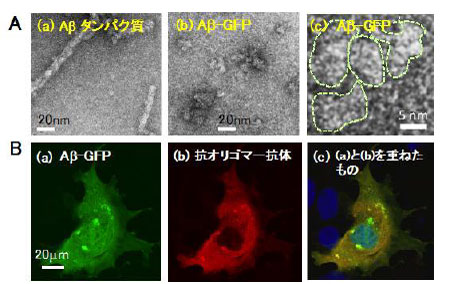
図1 生体内・生体外でのAβ−GFPの様子 |
(A)Aβタンパク質(a)とAβ-GFP(b、c)の電子顕微鏡像。Aβタンパク質は重合が進み繊維状になるのに対し、Aβ-GFPは重合が途中で止まり、数量体のオリゴマーを形成する(cの破線で囲まれた部分はそれぞれ1個の重合体を示す)。
(B)Aβ-GFPを発現させたCOS7細胞(a)を、オリゴマーだけを認識する抗体で染色した像(b)。 (a)と(b)がほぼ一致することから(c)、Aβ−GFPがオリゴマーであるとわかる。 |
また、AβとGFPを繋ぐリンカーが短いと、重合の影響を受けてGFPの蛍光は観察されなくなる。そこで今回発見した現象を利用して重合の状態が検出できるシステムを考案し、GFPの蛍光強度を利用した治療薬候補物質のスクリーニングが可能であることを実証した(図2)。GFP単独を特定の神経細胞に発現させたトランスジェニック線虫では神経細胞内に明瞭な蛍光が観察できる(図2a)が、2個のアミノ酸からなる短いリンカーを持つAβ-GFPを発現させた線虫では、Aβの重合の影響を受けてGFPの蛍光は観察されなかった(図2b)。この線虫を、Aβの重合を抑制するクルクミンを加えた培地で飼育した結果、GFPの蛍光が観察できた(図2c)。このように、Aβ-GFPは蛍光強度の変化を測定することで、Aβの重合を抑える創薬候補物質のスクリーニングに利用できる。
 |
|
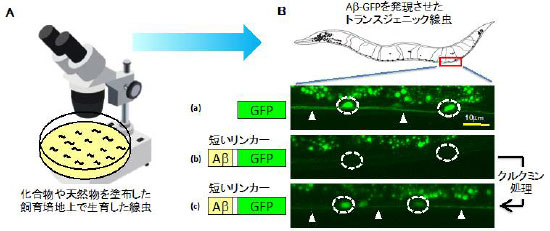
図2 生体を用いた創薬候補物質のスクリーニング例 |
|
飼育培地上の線虫(A)を顕微鏡で観察すると、クルクミンによるAβの重合抑制によって蛍光強度が増加した神経細胞を見ることができる(B)。白丸は神経細胞の細胞体、矢頭は神経細胞の軸索を示す。 |
今後は培養神経細胞を用いて、Aβ-GFPの蛍光強度を利用したアルツハイマー病の治療薬や予防薬の候補となる物質をより簡便にスクリーニングできる方法の開発に着手する。また、今回開発したAβ-GFPを発現させたトランスジェニックマウスを用いて、アルツハイマー病発症のごく初期に起こる神経細胞内部での微細な変化にAβオリゴマーが与える影響についてより詳細な解析を行い、アルツハイマー病発症のメカニズムの解明や予防に関する研究をすすめる。